1. Introduction
2. Materials and Methods
2.1 Microorganisms
2.2 Media Preparation and Cultivation
2.3 Preparation of Cordyceps militaris Extract
2.4 Antimicrobial Activity and Growth Analysis
3. Results and Discussion
1. Introduction
동충하초는 곤충에 기생하는 자낭균류에 속하는 균류로서, 숙주 곤충 체내에서 균사 형태로 생존하다가 일정한 환경 조건에서 숙주를 사멸시키고 체외로 자실체를 형성하는 독특한 생활사를 나타낸다[1]. 이러한 생태적 특징은 ‘겨울에는 곤충, 여름에는 풀’이라는 의미의 명칭으로 표현되어 왔다. 초기에는 박쥐나방 유충에 기생하는 Cordyceps sinensis를 중심으로 사용되었으나, 현재는 다양한 절지동물 및 기타 숙주에 기생하는 관련 균류를 포함하는 개념으로 확장되어 적용되고 있다[2]. 번데기 동충하초(Cordyceps militaris), 매미다발 동충하초(Cordyceps sobolifera), 눈꽃 동충하초(Paecilomyces japonica), 나방 동충하초(Cordyceps isarioides) 등은 대표적으로 보고된 종이다[2]. 곤충 기생성 균류는 전 세계적으로 약 800종 이상이 보고되었으며, 이 가운데 상당수가 동충하초목(Hypocreales)에 속한다[3,4]. 국내에서도 다양한 종이 확인되어 왔으며, 생물자원으로서의 가치가 지속적으로 평가되고 있다[3,4]. 특히 C. sinensis는 해발 3,000 m 이상의 고산 지대에서 제한적으로 자생하는 특성 때문에 희소성이 높고 경제적 가치가 큰 종으로 인식되어 왔다. 그러나 자연 채집에 의존하는 생산 구조와 과도한 채취는 자원 고갈 및 가격 상승 문제를 초래하였다[5]. 이러한 한계를 극복하기 위해 인공 재배 기술이 개발되었으며, C. militaris는 고체 및 액체 배양 시스템을 이용한 대량 생산이 가능하여 산업적 활용이 활발히 이루어지고 있다[6,7,8]. 국내에서는 P. japonica와 C. militaris가 식품 소재로 인정받고 있으며, C. militaris는 C. sinensis와 유사한 생리활성 특성을 보이면서도 코디세핀 함량이 상대적으로 높아 대체 자원으로 주목받고 있다[6,7]. 동충하초에는 다양한 생리활성 화합물이 존재하며, 코디세핀, 코디세픽산, 에르고스테롤, 만니톨, 아데노신 및 다당류 등이 주요 성분으로 보고되었다[9,10]. 이 가운데 코디세핀은 nucleoside 유도체로서 가장 핵심적인 활성 물질로 간주된다. 선행 연구에 따르면 코디세핀은 면역 조절, 항균 및 항염증 활성, 지질 대사 개선, 항종양 효과 등 다양한 생리적 기능과 관련이 있는 것으로 제시되었다[11,12,13,14,15,16,17,18]. 또한 특정 해충 유충에 대한 독성 작용도 보고되어 생물학적 방제 소재로서의 가능성도 제시된 바 있다[19].
유산균 식품의 기원은 인류가 가축을 사육하기 시작한 시기로 거슬러 올라가며, 자연 발효를 통해 형성된 식품이 그 출발점으로 추정된다. 미생물의 존재가 관찰된 이후 발효 과정에 대한 과학적 이해가 축적되었고, 유산균이 발효 식품의 형성과 품질에 핵심적인 역할을 한다는 사실이 규명되었다. 이후 유산균과 장수의 관련성이 제시되면서 유산균 및 발효유에 대한 관심이 확대되었다[20]. 유산균은 그람양성, 카탈라제 음성의 비운동성 구균 또는 간균으로 분류되며, 당을 발효하여 주로 유산을 생성하는 특징을 가진다[21]. 이들은 15–45°C 범위에서 생육하며, 37°C에서 활발한 증식을 보인다. Lactobacillus, Lactococcus, Leuconostoc, Streptococcus, Enterococcus 등을 포함한 여러 속이 존재하며, 이들 중 일부는 유제품 발효에 핵심적으로 활용된다. 유산균은 유기산 및 박테리오신 등의 대사산물을 생성하여 식품의 풍미 형성과 조직감 개선에 기여하며, 병원성 미생물의 증식을 억제하여 저장성을 향상시킨다[22]. 또한 인체에 유익한 기능을 나타내는 균주는 프로바이오틱스로 분류되며, 장내 미생물 균형 유지, 면역 기능 조절 및 대사 개선과 관련된 효과가 보고되고 있다[21,23,24].
최근 외식 산업, 단체 급식의 확대, 그리고 식생활의 다양화는 식중독 발생 증가와 밀접한 관련이 있는 것으로 보고되었다[25]. Salmonella spp., Escherichia coli, Vibrio parahaemolyticus, Bacillus cereus, Listeria monocytogenes, Staphylococcus aureus, Clostridium perfringens 등은 대표적인 식중독 원인균으로 지목된다[26,27]. 한편 항생제 사용의 확대는 내성균의 출현을 가속화하였으며, VRSA, MRSA, MRPA 등 다제내성균이 공중보건 문제로 대두되고 있다[28]. 이에 따라 합성 항균제의 대안으로 천연 유래 항균 물질에 대한 관심이 증가하고 있다[29,30]. 이러한 배경에서 본 연구에서는 C. militaris를 활용하여 천연 항균 소재로서의 적용 가능성을 평가하고자 하였다. 또한 동충하초 성분이 유산균의 생육 및 기능성 발현에 미치는 영향을 분석하여 프리바이오틱스적 활용 가능성 도 함께 검토하고자 하였다.
2. Materials and Methods
2.1 Microorganisms
한국미생물보존센터(KCCM)로부터 유산균 4종(Lactobacillus plantarum KCCM 11322, Lactobacillus acidophilus KCCM 32820, Lactobacillus lactis KCCM 34717, Weissella cibaria KCCM 41287)과 병원성균 4종(Escherichia coli KCCM 11569, 11587, 11591, 11596)을 분양 받아 사용하였다.
2.2 Media Preparation and Cultivation
유산균은 MRS broth(Difco, Sparks, USA), 병원성균은 LB broth(Difco, Sparks, USA)를 사용하였으며, 모든 배지는 121°C에서 20 min 멸균 후 사용하였다. 유산균은 10 mL 배지에 2% 접종하여 24 h 예비 배양하였으며, L. plantarum과 L. acidophilus는 37°C, L. lactis, W. cibaria는 30°C에서 배양하였다. 병원성균은 동일 조건으로 2% 접종 후 37°C에서 24 h 배양하여 실험에 이용하였다.
2.3 Preparation of Cordyceps militaris Extract
Cordyceps militaris 은 농업법인 투엘로부터 구입하였으며, 70% 에탄올을 10배 혼합하여 48시간 실온으로 추출하였다. 추출이후 여과지(Whatman No. 1, Tokyo, Japan))을 통하여 여과하고 감압농축기(Eyela, Tokyo, Japan)를 통하여 농축하였다. 농축물은 0.45 µm syringe filter(Advantec, Tokyo, Japan)로 여과하여 4°C에서 보관하며 시험에 사용하였다.
2.4 Antimicrobial Activity and Growth Analysis
동충하초 추출액의 항균 활성과 균주 생장에 대한 영향은 한천 확산법과 96-well microplate 법으로 평가하였다. 한천 확산법에서는 MRS 또는 LB broth에 0.75% agar를 첨가하여 멸균 후 각각 유산균 또는 병원성균을 0.25% 접종하여 평판을 제조하였다. 추출액은 원액 100%, 50%, 25%, 12.5%로 희석하여 멸균 paper disc(Advantec, Tokyo, Japan)에 40 µL씩 처리하였으며, 37°C에서 배양 후 저해환 형성을 확인하였다. 한편 96-well microplate 법에 의한 생장 분석은 Park and Lee [31]의 방법을 일부 수정하여 수행하였다. 유산균은 영양 조건을 조절하기 위해 1/2 농도의 MRS broth를 사용하였으며, 병원성균은 LB broth를 사용하였다. 각 well에 동충하초 추출액을 최종 농도 20%, 10%, 5% 및 2.5%로 첨가하고, 균주는 0.5% 접종하였다. 유산균은 균주 특성에 따라 30°C 또는 37°C에서, 병원성균은 37°C에서 배양하였다. 생장 변화는 microplate reader (Bio-Rad, USA)를 이용하여 655 nm에서 6 h 간격으로 측정하였다.
3. Results and Discussion
동충하초(Cordyceps militaris) 추출액의 생장 활성은 유산균 4종과 Escherichia coli 4종을 대상으로 paper disc법과 96-well microplate 법으로 평가하였다. 추출액은 원액부터 12.5%까지 단계적으로 희석하여 처리하였다. 그 결과, 유산균에서는 모든 농도에서 저해환이 관찰되지 않았으며(Fig. 1), 병원성균에서도 명확한 저해환이 형성되지 않았다(Fig. 2). 이는 동충하초 추출액 내 항균 성분이 한천 배지에서 충분히 확산되지 않았거나, 고체 배지 환경에서는 활성 발현이 제한되었을 가능성을 시사한다. 또한 동충하초 유래 성분이 정균적(bacteriostatic) 작용을 나타내는 경우, 확산법에서는 뚜렷한 저해환으로 확인되지 않을 수 있다. 이에 따라 본 연구에서는 액상 배양 조건에서의 생장 변화를 96-well microplate 법으로 분석하였다(Fig3과 4). 배양배지의 농도는 원 배지농도와 1/2로 조정하였다. 그 이유는 각 미생물에 제공된 배지는 최적배지이기 때문에 배양의 성장증식의 경우 추출물의 첨가 효과를 밝히기에는 어렵기 때문이다. 그러나 항균작용의 경우는 최적의 배지에서 추출물의 첨가 효과를 알 수 있다. 배지의 성분함량을 1/2낮춘 조건에서는 모든 유산균에서 동충하초 추출액 첨가에 따른 생장 촉진 효과가 뚜렷하게 나타났다(Fig. 3). 특히 L. acidophilus KCCM 32820은 1/2 MRS 조건에서 현저한 증식 증가를 보였고, 다른 균주들 역시 대조군 대비 현저한 생장 증가를 나타냈다. 이러한 결과는 동충하초 추출액이 유산균에 대해 단순한 항균 작용이 아니라 선택적 생장 촉진 효과를 나타낼 수 있음을 의미한다. 특히 영양이 제한된 환경에서 생장 촉진 효과가 더욱 두드러졌다는 점은, 동충하초 유래 성분이 추가적인 탄소원, 질소원 또는 생리활성 인자로 작용했을 가능성을 시사한다. Cordycepin과 같은 nucleoside 계열 물질이나 다당류 성분은 세포 대사 조절 또는 에너지 이용 효율 개선에 관여할 수 있으며, 이로 인해 유산균의 증식이 촉진되었을 가능성이 있다. 이러한 경향은 동충하초가 프리바이오틱스적 특성을 가질 수 있음을 뒷받침한다. 한편, E. coli KCCM 11569, 11587, 11591 및 11596은 모든 농도에서 생장이 억제되었다(Fig. 4). 이는 동충하초 상등액이 일부 그람음성 병원성균에 대해 억제 효과를 가질 수 있음을 보여준다. 또한 동충하초 유래 활성 성분이 특정 균주에서는 성장 억제 경로를 활성화시키는 반면, 다른 균주에서는 이용 가능한 기질로 활용되었을 가능성도 고려할 수 있다. 이러한 차이는 세포막 투과성, 대사 특성 또는 스트레스 반응 조절 기전의 차이와 관련될 수 있다. 선행 연구에서도 Cordyceps militaris는 특정 세균에 대해 선택적으로 항균 활성을 나타내는 것으로 보고되었으며[4], cordycepin은 일부 장내 세균에 대해 억제 효과를 보이면서 Lactobacilli의 생장에는 부정적 영향을 미치지 않는 것으로 알려져 있다[32]. 본 연구에서 관찰된 유산균 생장 촉진 및 E. coli 억제 결과는 이러한 선택적 작용 특성과 일치하는 경향을 보인다. 종합하면, 동충하초 추출액은 고체 배지 확산법에서는 항균 활성이 확인되지 않았으나, 액상 배양 조건에서는 유산균의 생장을 촉진하고 실험 병원성균의 증식을 억제하는 선택적 생장 조절 효과를 나타냈다. 이는 동충하초가 천연 항균 소재이면서 동시에 프리바이오틱스적 기능을 갖는 잠재적 기능성 자원임을 시사한다. 다만, 활성 성분의 규명 및 작용 기전에 대한 추가 연구가 필요하다.

Fig. 1
Antibacterial activity against lactic acid bacteria by adding of Cordyceps militaris extract using the paper disc method. A, Lactobacillus acidophilus KCCM 32820; B, Lactobacillus plantarum KCCM 11322; C, Lactobacillus lactis KCCM 34717; D, Weissella cibaria KCCM 41287. a, 40 µL Cordyceps militaris extract; b, 20 µL Cordyceps militaris extract; c, 10 µL Cordyceps militaris extract; d, 5 µL Cordyceps militaris extract.

Fig. 2
Antibacterial activity against Escherichia coli by adding of Cordyceps militaris extract using the paper disc method. A, E. coli KCCM 11569; B, E. coli KCCM 11587; C, E. coli KCCM 11591; D, E. coli KCCM 11596. a, 40 µL Cordyceps militaris extract; b, 20 µL Cordyceps militaris extract; c, 10 µL Cordyceps militaris extract; d, 5 µL Cordyceps militaris extract.
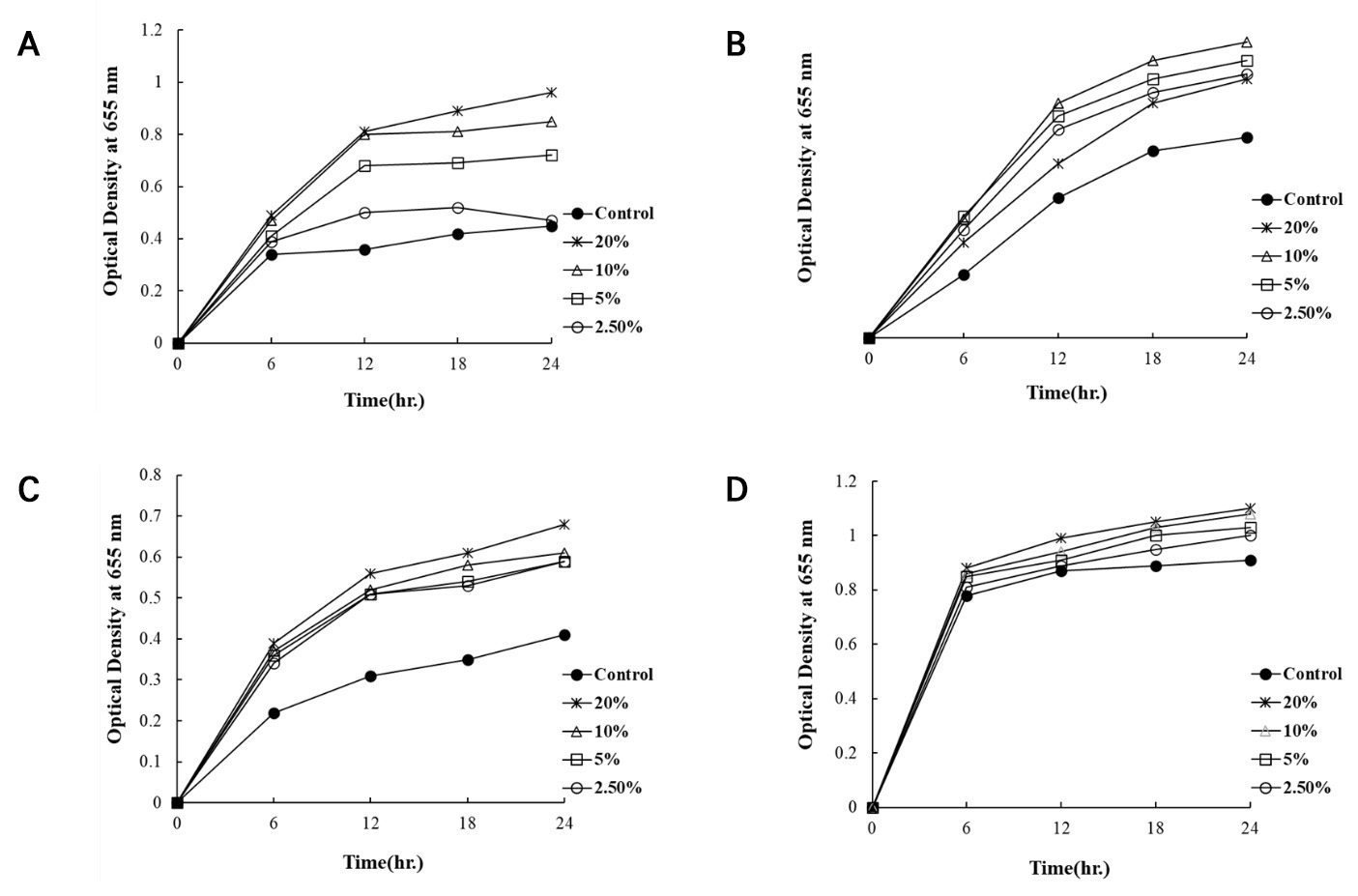
Fig. 3
Growth effect of lactic acid bacteria by adding Cordyceps militaris extract using the 96 well plate method. Cordyceps militaris extract was added at final concentrations of 20%, 10%, 5%, and 2.5%, and bacterial growth was monitored by measuring optical density at 655 nm during incubation. A, Lactobacillus acidophilus KCCM 32820; B, Lactobacillus plantarum KCCM 11322; C, Lactobacillus lactis KCCM 34717; D, Weissella cibaria KCCM 41287.
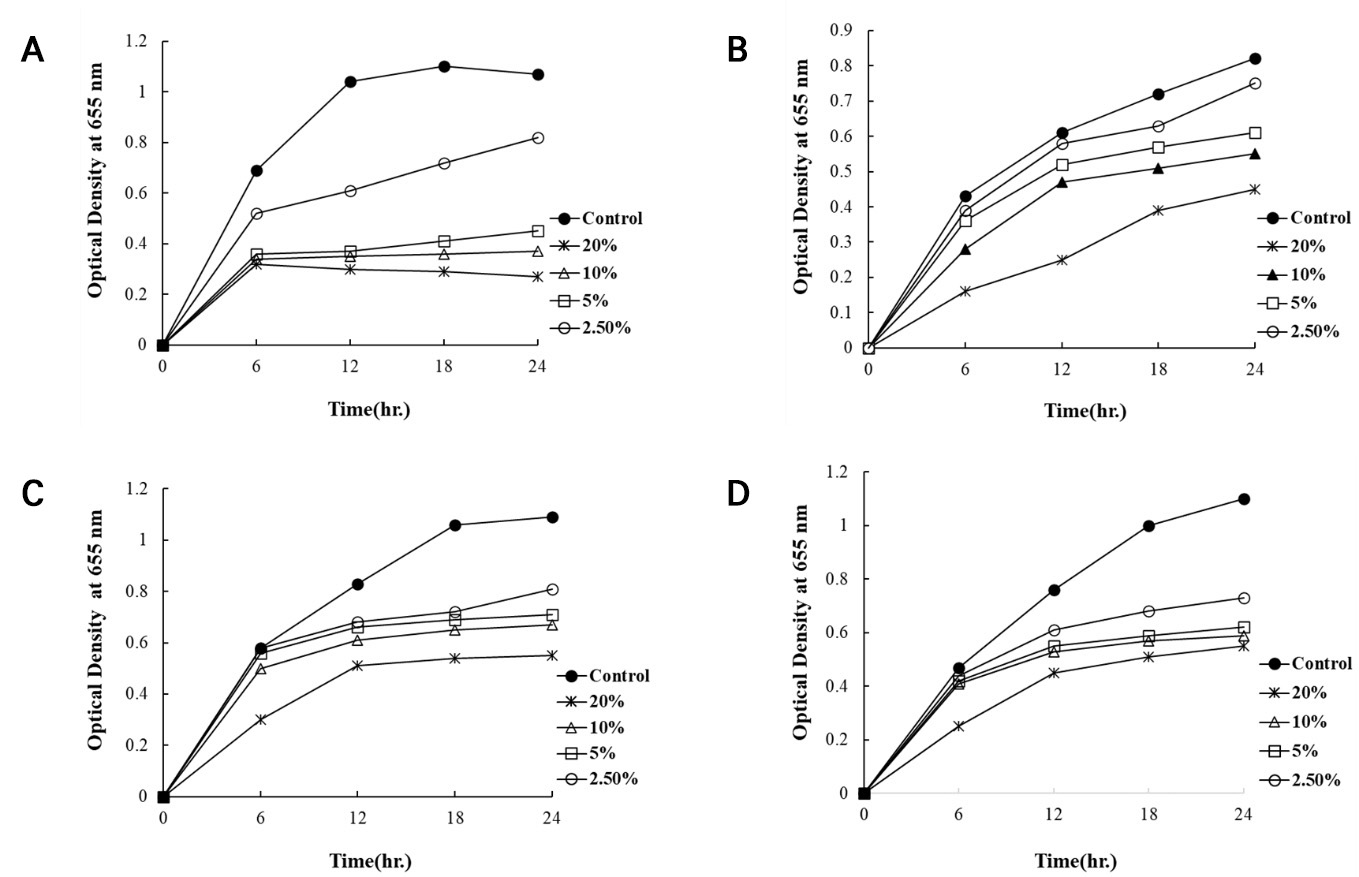
Fig. 4
Growth effect of Escherichia coli by adding Cordyceps militaris extract using the 96 well plate method. Cordyceps militaris extract was added at final concentrations of 20%, 10%, 5%, and 2.5%, and bacterial growth was monitored by measuring optical density at 655 nm during incubation. A, E. coli KCCM 11569; B, E. coli KCCM 11587; C, E. coli KCCM 11591; D, E. coli KCCM 11596.
동충하초의 주요 성분과 생리활성에 관한 선행 연구들은 본 연구 결과를 해석하는 데 근거를 제공한다. Lewis와 Smith [33]는 동충하초에서 탄수화물을 분석한 결과 유리당 가운데 만니톨의 함량이 가장 높다고 보고하였다. Reis 등[34]은 C. militaris에서 확인된 유리당으로 만니톨(2.01 g/100 g dw)과 트레할로스(24.71 g/100 g dw)를 보고하였으며, 특히 트레할로스의 함량이 더 높은것으로 나타났다. 또한 유기산분석에서는 구연산이 가장 높은 함량(7.97 g/100 g dw)으로 검출되었고, 옥살산(0.33 g/100 g dw)과 푸마르산(0.13 g/100 g dw)도 정량 가능하였다고 보고하였다. 구연산과 푸마르산은 Krebs 회로에서 중요한 역할을 하는 유기산으로 알려져 있다. 구연산은 골조직에서 결정 형성을 촉진하는 물질로 보고되었으며[35], 푸마르산은 항염증, 신경보호 및 화학예방 활성과 같은 다양한 생리적 효과를 나타낸다. 또한 과일 및 채소 저장과정에서 항균제로 작용할 수 있는 것으로 알려져 있다[36]. Reis 등[34]은 항균 활성 측면에서 C. militaris 메탄올 추출물이 Bacillus cereus(MIC 0.015 mg/ml; MBC 0.03 mg/ml)와 Pseudomonas aeruginosa(MIC 0.015 mg/ml; MBC 0.03 mg/ml)에 대해 가장 높은 항균 활성을 나타냈다고 보고하였다. Ahn 등[32]은 C. militaris의 배양 여과액, 메탄올 추출물 및 그 성분인 cordycepin이 Clostridium 종에 대해 강한 생육 억제 활성을 나타낸다고 보고하였다. 그러나 동일한 조건에서 8종의 유산 생성 세균의 생장에는 부정적 영향을 미치지 않는 것으로 나타났다. C. militaris로부터는 에르고스테롤과 다당류 등 다양한 약리 활성 물질이 분리된다. 이러한 물질들은 항염증, 항산화, 항종양, 항전이, 면역조절, 혈당강하, 스테로이드 생성 촉진 및 지질 저하 활성 등 다양한 생리적 효과를 나타내는 것으로 알려져 있다1. Zhong 등[38]은 C. militaris 유래 다당류를 종양 모델(S180 이식 마우스)에 적용한 결과 종양 성장을 억제되었으며, 동시에 화학요법에 따른 독성 효과도 감소하는 것을 확인하였다. Gim 등[39]은 갈색거저리 동충하초의 Streptococcus thermophilus KCCM 3782 유산균 발효과정에서 항산화 활성을 분석한 결과, 유산균 발효 후 항산화 효과가 증가한다고 보고하였다. 한편 동충하초의 항균 활성은 추출물의 종류와 시험균주에 따라 다르게 나타나는 것으로 보고되고 있다. Park 등[40]은 동충하초 추출물의 병원성 미생물(Bacillus subtilus KCTC 1659, Listeria monocytogenes ATCC 7644, Staphylococcus aureus ATCC 13565, Escherichia coli O157, Shigella sonnei KCTC 2009, Salmonella typhimurium ATCC 7988)에 대한 항균 효과를 분석하였다. 그 결과 균사체의 물추출물은 대부분 식중독균에 대해 항균 활성을 나타내지 않았으나, Listeria monocytogenes에 대해서는 1% 이상의 농도에서 항균 활성이 확인되었다. 반면 자실체 추출물에서는 항균 활성이 나타나지 않았다. Lee 등[4]은 번데기 동충하초와 눈꽃동충하초 추출물이 Bacillus cereus KACC 10004에서만 항균 활성을 나타냈으며, Listeria monocytogenes KACC 10764, Salmonella enterica KACC 10763, Escherchia coli KACC 10115, Pseudomonas aeruginosa KACC 10260에는 항균 활성이 나타나지 않았다고 보고하였다. 이러한 선행 연구들을 종합하면 동충하초 추출물의 항균활성 또는 미생물증식 조절 효과는 추출방법(상징액, 물추출물, 메탄올 추출물 등)과 시험 균주의 특성에 따라 크게 달라질 수 있음을 시사한다. 따라서 향후 연구에서는 동충하초 추출물 중 어떤 성분이 유산균의 생장 촉진 및 병원성균 억제에 기여하는지에 대한 규명이 필요하다. 특히 cordycepin, 다당류, 유리당 및 유기산과 같은 후보 성분의 정량분석과 함께 분획별 생리활성 평가가 요구된다. 또한 균주별 반응 차이를 설명하기 위해 막투과성변화, 에너지대사 조절 및 스트레스 반응 유도와 같은 작용 기전에 대한 추가적인 분석이 필요할 것으로 판단된다.




