1. Introduction
2. Materials and Methods
2.1. 공시동물 및 처리
2.2. 사료 및 음수 섭취량 및 체중 측정
2.3. DAI
2.4. 샘플링 및 위장관 길이의 측정
2.5. 분변 SCFAs 측정
2.6. RT-qPCR
2.7. 통계 분석
3. Results and Discussion
3.1. 체중, 섭취량 및 DAI 변화
3.2. 위장관 길이
3.3. 분변의 SCFAs
3.4. RT-qPCR
4. Conclusion
1. Introduction
염증성 장 질환(Inflammatory bowel disease, IBD)은 유전, 면역, 환경 및 장내 미생물 등의 요인에 의해 발생하는 만성 염증성 질환이다[1,2]. 이는 선진국과 개발도상국을 중심으로 하여 전세계적으로 발생률과 유병률이 증가하고 있으며, 복통, 설사, 혈변 등의 주요 임상 증상을 동반하여 삶의 질을 크게 저하시킨다[3,4,5]. 현재 IBD의 치료를 위하여 다양한 약리학적 접근이 시도되고 있다[6,7]. 그러나 대부분의 치료제는 설사, 두통, 알레르기, 복통, 위장장애 등 여러 부작용을 초래할 수 있으며, 약물 내성 및 높은 치료 비용 등의 문제를 동반한다[8,9,10]. 이에 따라 부작용이 적고 장기적인 섭취가 가능하며, 항염증 및 면역 조절 효능을 가진 천연 기능성 소재의 발굴에 관한 연구가 활발히 진행되고 있다[11,12].
동충하초(Cordyceps militaris, CM)는 동아시아에서 오랫동안 약용 버섯으로 사용되어 왔으며, cordycepin, adenosine, polysaccharides 등 다양한 생리활성 물질을 함유하고 있다[13]. 이러한 성분은 강력한 항산화 및 항염증 활성을 나타낼 뿐만 아니라, 면역 조절 기능을 수행하는 것으로 보고되었다[14]. 특히 CM에 포함된 polysaccharides는 장내 미생물의 단쇄지방산(Short-chain fatty acids, SCFAs) 생성을 촉진하여 장 장벽 기능 강화 및 염증 완화에 기여할 수 있는 잠재력을 가진다[15,16]. 최근에는 이러한 CM의 기전에 주목하여 IBD를 개선할 수 있다는 가능성이 제기되고 있으나[17,18], 유효 성분이 복합적으로 함유된 동충하초 분말(Cordyceps militarispowder, CMP) 형태가 고농도 Dextran sulfate sodium (DSS)로 유도된 급성 대장염 모델에 미치는 영향에 대한 연구는 부족한 실정이다.
이에 본 연구에서는 DSS를 이용해 유도한 대장염 마우스 모델에서 CMP를 음수에 혼합 급여하여, 대장염의 예방 및 개선 효과를 평가하고자 한다. 이를 위하여 CMP 섭취가 체중 및 질병활동지수(Disease activity index, DAI) 변화, 위장관 길이, 분변 내 SCFAs 조성, 장 조직의 밀착연접 유전자 발현에 미치는 영향을 종합적으로 분석하였다. 이를 통해 CM의 대장염 완화 효능을 평가하고, CM 기반 IBD 예방 및 치료 전략 개발을 위한 기초 자료를 제공하고자 한다.
2. Materials and Methods
2.1. 공시동물 및 처리
본 연구는 한경국립대학교 동물생명윤리위원회의 승인(IACUC 승인 번호: 2024-19)을 받아 수행되었다. 실험에는 6주령 수컷 ICR 계통 마우스 40마리(나라바이오텍, 서울, 대한민국)를 사용하였으며, 모든 개체는 실험 시작 전 1주간의 적응 기간을 거친 후 7주령 시점부터 처리를 진행하였다. 실험 개시 시 마우스의 평균 체중은 31.89 ± 0.20 g이었다. 사육 환경은 12시간 명암 주기(08:00 점등), 실내 온도 23 ± 2°C, 상대습도 40−60%로 일정하게 유지하였다. 사료 및 음수는 자유급여(ad libitum) 방식으로 제공하였다. 실험 설계는 DSS 처리 여부와 CMP 급여 여부를 요인으로 하는 2 × 2 요인 배열로 구성하였다. 총 40마리는 그룹당 10마리씩 무작위 배정하였으며, 처리군은 다음과 같다: (1) A군: 무처리 대조군(Control), (2) B군: CMP 급여군, (3) C군: DSS 급여군, (4) D군: DSS와 CMP 병행 급여군. 처리 물질 DSS(대정화금, 시흥, 대한민국)는 분자량이 40,000 Da였으며, 5% 농도로 음수에 혼합하여 제공하였다. DSS 음수는 실험 기간 동안 매일 08:00에 신선하게 교체하였다. CMP(투엘, 광주, 대한민국)은 100 mg/kg의 농도로 희석하여 DSS 처리 여부와 상관없이 지정된 그룹에 음수 형태로 급여하였다. 모든 처리는 총 7일간 실시하였으며 실험 기간 동안 마우스의 건강 상태 및 행동 변화는 매일 관찰하였다.
2.2. 사료 및 음수 섭취량 및 체중 측정
사료섭취량과 음수섭취량은 실험 기간 동안 매일 측정하였다. 매일 오전 동일한 시점에 사료와 음수를 새로 제공하였으며, 전일 제공량에서 잔량을 제외하여 개체별 섭취량을 산출하였다. 산출된 값은 실험 기간 동안의 평균 일일 사료섭취량과 평균 일일 음수섭취량 계산에 활용하였다. 체중은 전자저울을 이용하여 실험 시작일과 종료일에 각각 측정하였으며, 추가적으로 매일 체중을 기록하여 개체별 체중 변화 양상을 확인하였다.
2.3. DAI
DAI는 실험 기간 동안 매일 체중 측정과 육안적 관찰을 통해 평가하였다. DAI 산출을 위해 체중 변화, 대변의 상태(농도), 및 대변 출혈 여부를 점수화하였으며, 각 항목의 점수를 합산하여 최종 점수를 산정하였다. 체중 변화 점수는 Wu 등[18]의 기준에 따라 부여하였다. 체중 감소가 없는 경우 0점, 1−5% 감소 시 1점, 5% 초과 10% 이하 감소 시 2점, 10% 초과 15% 이하 감소 시 3점, 15% 초과 20% 이하 감소 시 4점으로 평가하였다. 대변 점수는 Liu 등[19]의 방법을 참고하여 대변 농도와 출혈 여부로 구분하여 평가하였다. 대변 농도는 정상 변 0점, 묽은 변 2점, 설사 4점으로 부여하였으며, 대변 출혈은 혈흔이 없을 경우 0점, 혈액이 미량 관찰되는 경우 2점, 육안으로 명확히 출혈이 관찰될 경우 4점으로 평가하였다. 최종 DAI는 체중 변화 점수, 대변 농도 점수, 출혈 점수를 합산하여 산출하였으며, 총점은 0−12점 범위에서 기록하였다.
2.4. 샘플링 및 위장관 길이의 측정
실험 기간 동안 매일 배설된 대변 샘플을 수집하여 분석 전까지 –80°C에 보관하였다. 실험 종료일(7일째)에는 모든 마우스를 24시간 절식시킨 후, 8일차 오전에 경추 탈골법을 이용하여 인도적으로 안락사하였다. 안락사 직후 복부를 에탄올로 소독한 뒤 개복하여 위장관을 적출하였다. 이후 위에서부터 대장 말단까지의 전체 위장관 길이를 측정하였으며, 대장 길이 또한 별도로 기록하였다. 길이 측정 후 소장을 위장관에서 분리하여 공장(jejunum)을 채취하였다. 채취돈 공장 조직은 RT-qPCR 분석을 위해 장 내용물을 PBS를 이용하여 조심스럽게 세척해준 뒤, –196°C의 액체질소에 급속동결 후, –80°C에 보관하였다.
2.5. 분변 SCFAs 측정
대변 내 SCFA 분석을 위해 –80°C에서 보관된 샘플을 해동한 후 가스크로마토그래피-질량분석기(GC-MS)를 이용하여 분석하였다. 전처리는 대변 샘플 0.7 g에 0.8 mL의 50% H2SO4(삼전화학, 서울, 대한민국)을 첨가한뒤, 즉시 2 mL의 Ethyl ether(삼전화학, 서울, 대한민국)를 추가하여 SCFAs를 추출하는 방식으로 수행하였다. 혼합 용액은 볼텍싱 후 3,000 × g에서 10분간 원심분리하였으며, 상층액을 회수하여 0.22 µm 실린지 필터(Jet Biofil, 광저우, 중국)를 이용해 vial(Zeal Science, 뉴사우스웨일스, 호주)에 여과하였다. 이후 vial cap(Agilent Technologies, 산타클라라, 미국)으로 vial을 잠가주었다. 정량 분석을 위해 acetic acid, propionic acid, butyric acid(Sigma-Aldrich, 세인트루이스, 미국)를 표준물질로 사용하였으며, 0−3000 ppm 범위에서 검량선을 작성하였다. 이를 위해 표준용액은 10, 50, 100, 300, 500, 1,000, 2,000, 3,000 ppm 농도로 제조하였다. GC-MS 분석은 Shimadzu GCMS-QP2020NX(Shimadzu Scientific Korea, 서울, 대한민국)를 이용하여 수행하였다. 분리는 SH-PolarD capillary column (0.32 mm × 1 µm × 60 m)을 사용하였으며, 이동상 가스로는 99.9% 고순도 헬륨(에어코리아, 여주, 대한민국)을 사용하였다. 시료는 280°C에서 split mode로 주입하였으며, carrier gas는 column flow mode로 설정하였다. 운반 가스 압력은 89.3 kPa였고, column flow rate는 2.0 mL/min이었다. GC 오븐 온도 조건은 초기 50°C에서 5분 유지 후 8°C/min의 속도로 240°C까지 상승시키고, 이후 5분간 유지하였다. MS 조건은 ion source 200°C, interface 230°C로 설정하였으며, 분석은 scan mode와 SIM mode 병행 방식으로 진행하였다. Scan mode의 m/z 범위는 25−400, 분석 시간은 4.00−30.00 min으로 설정하였으며 scan speed는 1428이었다. SIM 분석에서는 m/z 29.00, 46.00, 45.00, 43.00, 60.00, 74.00, 28.00, 73.00, 41.00, 87.00를 사용하여 SCFAs 정성·정량 분석을 수행하였다. 최종적으로 분석된 크로마토그램에서 피크 면적을 검량선에 적용하여 개별 SCFAs 농도를 산출하였다.
2.6. RT-qPCR
RT-qPCR 분석을 위해 각 그룹의 공장(jejunum) 샘플에서 총 RNA를 추출하였다. 조직은 –80°C에서 보관된 후 액체질소 하에서 분쇄하였으며, TRIzolⓇ 시약(Thermo Fisher Scientific Korea, 서울, 대한민국)을 이용하여 RNA를 추출하였다. 조직 100 mg당 TRIzolⓇ 시약 1 mL를 첨가한 뒤, 호모게나이저(SHG-15D, DAIHANⓇ, 강원, 대한민국)를 이용하여 균질화하였다. 균질화된 시료는 4°C에서 12,000 × g로 5분간 원심분리한 후 상층액을 새로운 튜브에 분리하였다. 이후 5분간 상온 반응 후 클로로포름 0.2 mL (Thermo Fisher Scientific Korea, 서울, 대한민국)를 첨가하여 혼합한 뒤 12,000 × g에서 15분간 원심분리하였다. 상층액을 분리하여 70% 이소프로판올 0.5 mL(Sigma-Aldrich, 세인트루이스, 미국)를 첨가하고, 4°C에서 10분간 반응 후 12,000 × g에서 10분간 원심분리하여 RNA를 침전시켰다. 침전물은 70% 에탄올(Thermo Fisher Scientific Korea, 서울, 대한민국) 1 mL로 세척한 뒤 7,500 × g에서 5분간 원심분리하였다. 이후 상층액을 제거하고 상온에서 5−10분간 건조한 후 50 µL의 RNase-free water(Thermo Fisher Scientific Korea, 서울, 대한민국)를 첨가하여 용해하였다. RNA 용해는 60°C로 설정된 WiseBath®(SciLab®, 서울, 대한민국)를 이용해 10분간 수행하였으며, 완성된 RNA는 사용 전까지 –80°C에서 보관하였다. cDNA 합성은 추출한 총 RNA를 주형으로 하여 RR092B PrimeScript™ FAST RT reagent Kit with gDNA Eraser (Takara Korea, 서울, 대한민국)를 사용하였으며 제조사 프로토콜에 따라 수행하였다. RT-qPCR 분석은 qTOWER3G 시스템(Analytik Jena Korea, 서울, 대한민국)을 사용하였으며, RR830B, TB Green® Premix Ex Taq™ II FAST qPCR Kit(Takara Korea, 서울, 대한민국)를 이용하였다. 분석 유전자는 밀착연접 관련 유전자인 ZO-1 (Zonula Occludens-1), CLDN4 (Claudin-4), OCLN (Occludin)이었으며, 기준유전자로 β-actin을 사용하였다. 모든 프라이머는 PRECAREGENE(경기, 대한민국)에서 합성하였으며, 서열 정보는 Table 1에 제시하였다.
Table 1.
Primers used for RT-qPCR
| Gene | Sequences (5’ → 3’) | Product size | GenBank accesstion number |
| ZO-11) | F: GAGCAAGCCTTCTGCACATC | 201 | NM_001163574.2 |
| R: CTGTACTGTGAGGGCAACGG | |||
| OCLN2) | F: GGTGAATGGGTCACCGAGGG | 238 | NM_001360534.1 |
| R: GACTTTCAAAAGGCCTCACGG | |||
| CLDN43) | F: CCATGGAACCCTTCCGTTGA | 189 | NM_009903.2 |
| R: GCAAGACAGTGCGGAAAAGG | |||
| β-actin | F: GTGCTTCTAGGCGGACTGTT | 242 | NM_007393.5 |
| R: TTTGCTCCAACCAACTGCTG |
2.7. 통계 분석
실험 결과는 2 × 2 요인 설계를 기반으로 이원분산분석(Two-way ANOVA)을 수행하여 처리 요인 간 및 상호작용 효과를 평가하였다. 처리군 간 평균 비교는 Tukey 사후검정(Tukey’s post hoc test)을 적용하여 유의성을 확인하였다. 통계적 유의수준은 p < 0.05로 설정하였으며, 0.05 < p ≤ 0.10의 경우 통계적 경향성이 있는 것으로 판단하였다. 모든 통계 분석은 SAS 9.4 software를 사용하여 수행하였다.
3. Results and Discussion
3.1. 체중, 섭취량 및 DAI 변화
실험 기간 동안의 체중 변화, 사료 및 음수 섭취량, 그리고 DAI 결과는 Table 2에 제시하였다. 실험 개시 체중은 처리구 간 유의적 차이가 없었으나, 평균 일일 사료 섭취량은 DSS 처리에 의해 C와 D군에서 유의적으로 감소하였다(p < 0.05). 평균 일일 음수 섭취량 또한 DSS 처리에 의해 C와 D군에서 유의적으로 감소하였으며(p < 0.05), CMP 급여에 따라 감소하는 경향을 보였다(p = 0.08). 종료 체중 역시 DSS처리에 의해 유의적으로 감소하는 결과를 나타내었다(p < 0.05).
Table 2.
Changes in body weight, average daily feed intake, average daily water intake and disease activity index across treatment groups
선행 연구에 따르면, DSS로 유도된 대장염 모델 마우스에서는 장 염증으로 인한 체중 감소가 발생하는 것으로 보고되었다[20,21]. 본 연구에서도 DSS를 급여한 C와 D군에서 종료 체중이 유의적으로 감소하여 기존 연구와 일치하는 결과를 보였으며, 이는 DSS로 인한 장 염증이 체중 감소의 직접적인 원인임을 시사한다. 또한 DSS 처리군에서 관찰된 사료 및 음수 섭취량의 감소는 장염 유도 모델의 특징적인 생리 반응으로, 여러 연구에서 동일한 결과가 보고된 바 있다[22,23,24]. 따라서 본 연구에서의 섭취량 감소 역시 DSS 급여가 섭취 행태 전반에 부정적인 영향을 미친 것으로 판단된다.
한편, 본 연구에서는 CMP 급여가 음수 섭취량을 감소시키는 경향이 관찰되었다. 그러나 현재까지 CM이나 CMP의 급여가 섭취량을 감소시킨다는 일관된 증거는 보고된 바 없으며, 오히려 섭취량에 부정적 영향이 없거나 성장 능력이 개선된다는 보고가 다수이다[25,26]. 따라서 본 연구에서 관찰된 섭취량 감소는 CMP 자체의 식욕 저하 효과 보다는, CMP 특유의 쓴맛이 음수의 기호성을 저하시켜 섭취량 감소로 이어졌을 가능성이 높다[27,28,29].
DAI 변화를 살펴보면, Day 1과 Day 2에서는 처리구 간 유의적인 차이가 없었으나(p > 0.05), Day 3부터 Day 6까지 DSS 처리는 C군과 D군의 DAI를 유의적으로 증가시켰다(p < 0.05). 이는 DSS가 대장염을 효과적으로 유도했음을 보여준다[30,31]. 본 연구에서 100 mg/kg의 CMP 급여 효과는 Day 4부터 나타났으며, CMP가 보충된 B군과 D군은 이를 급여하지 않은 A군 및 C군에 비해 상대적으로 낮은 DAI를 유지하였다(p < 0.05). 특히 Day 4 이후 DSS와 CMP 간의 유의적인 상호작용 효과가 확인되었다. DSS 단독 처리군(C군)은 지속적으로 높은 DAI를 보인 반면, DSS와 CMP를 함께 투여한 D군에서는 DAI 증가가 억제되는 결과가 나타났다(p < 0.05). 이는 100 mg/kg CMP 경구 투여가 DAI를 개선시킨 Wu 등[18]의 연구 및 CM이 염증 반응을 억제하여 DAI를 개선한다는 보고와 일치한다[17,32]. 결론적으로 100 mg/kg의 CMP 급여는 DSS로 유도된 장 염증 및 임상 증상을 완화할 수 있음을 시사한다.
3.2. 위장관 길이
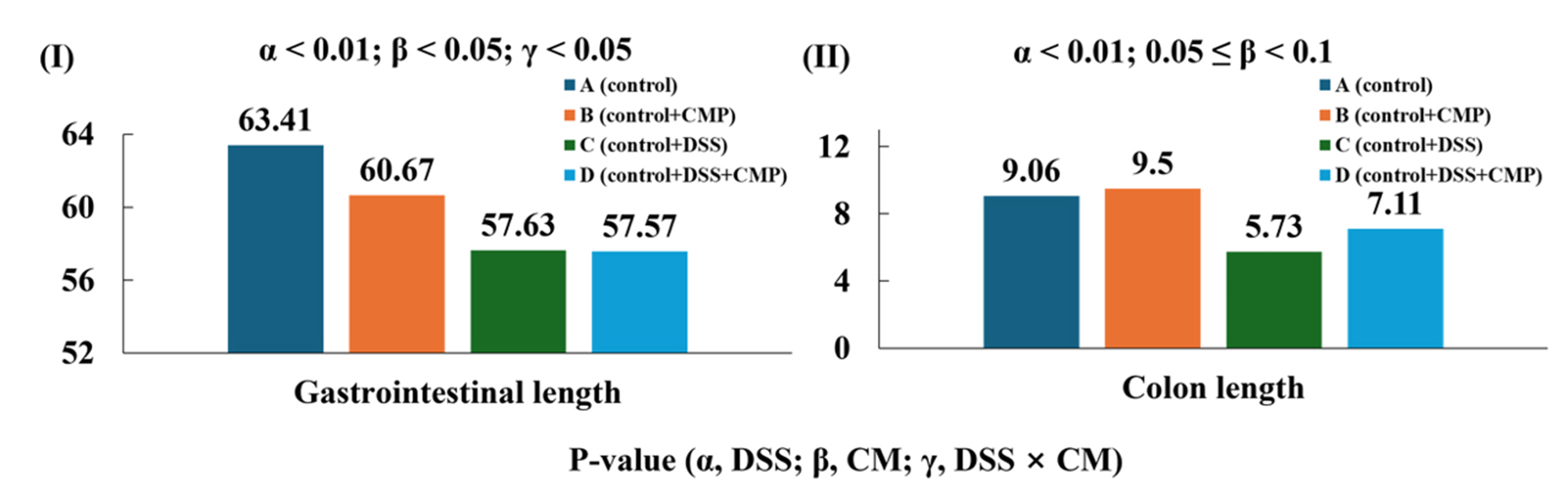
전체 장 길이와 대장 길이를 측정한 결과는 Fig. 1에 제시하였다. DSS 처리는 C, D군의 전체 장 길이와 대장 길이를 유의적으로 감소시켰다(p < 0.001). 이는 마우스에게 DSS로 대장염을 유도할 경우 위장관 및 대장 길이가 단축된다는 선행 연구 결과와 일치한다[33,34,35]. 반면, CMP 급여는 전체 장 길이에는 유의적인 영향을 미치지 않았으나, DSS 처리 조건에서 D군의 대장 길이를 증가시키는 경향을 나타내었다(p = 0.06). 또한 대장 길이에 있어 CMP와 DSS 간의 유의적인 상호작용 효과가 확인되었다(p < 0.05). 이러한 결과는 DSS 장염 모델 마우스에게 100 mg/kg의 CMP를 급여했을 때 대장 길이 감소가 완화되었다는 Wu 등[18]의 연구 및 500 mg/kg의 CM 추출물을 급여한 Park과 Park[17]의 연구 결과와 유사하다. 따라서 CMP는 DSS에 의해 유도된 대장의 구조적 손상을 부분적으로 완화하는 효과가 있는 것으로 판단된다.
3.3. 분변의 SCFAs
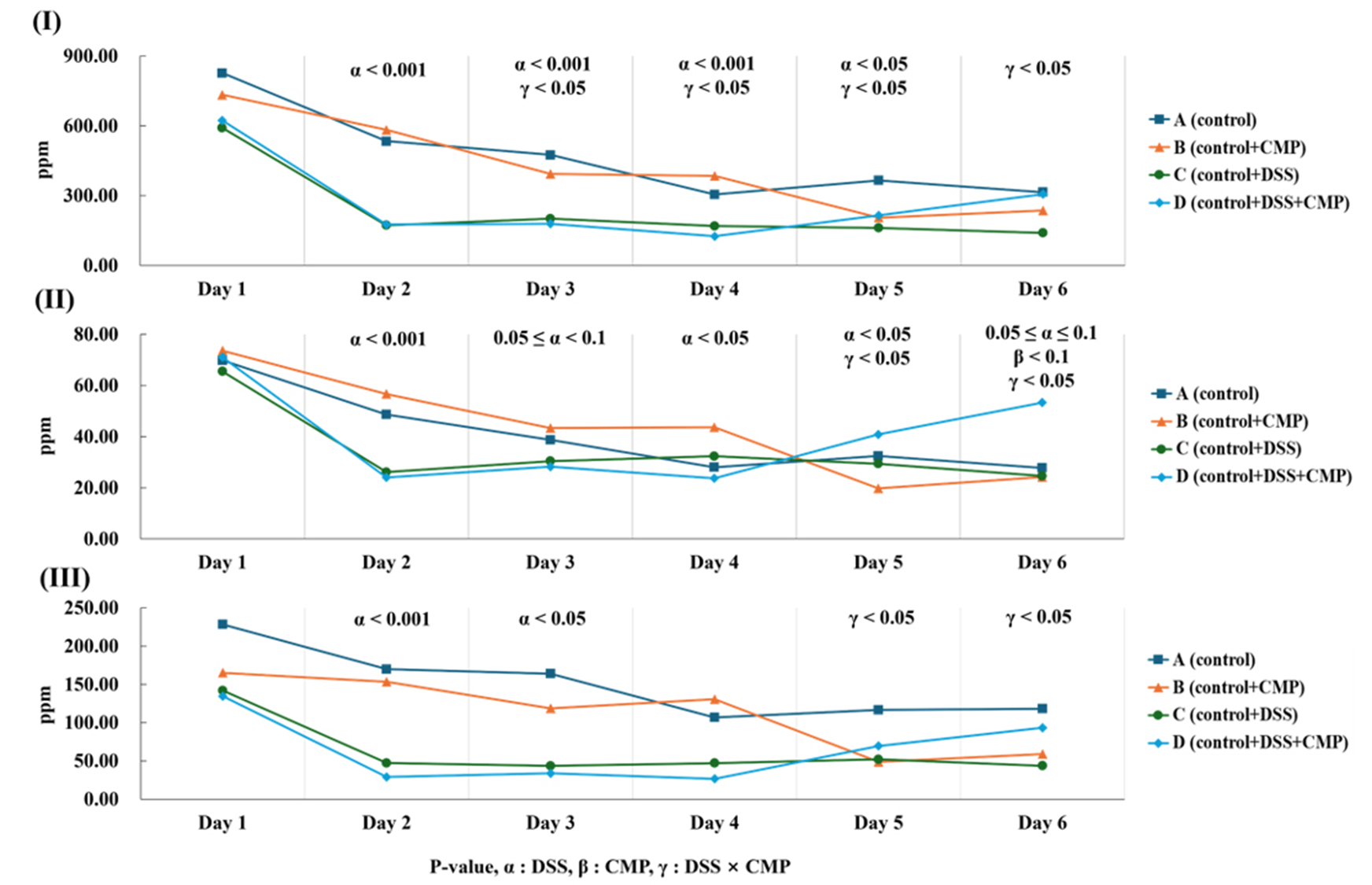
분변 내 SCFAs 측정 결과는 Fig. 2에 제시하였다. DSS 처리는 acetate, propionate 및 butyrate 농도 전반에 영향을 미쳤다. Acetate 농도는 Day 2−5 동안 C와 D군에서 유의적으로 감소하였으며(p < 0.05), propionate 농도 또한 Day 2−6 동안 감소하는 양상을 보였다(Day 2, 4, 5, p < 0.05; Day 3, p = 0.06; Day 6, p = 0.05). Butyrate 농도 역시 Day 2−4 동안 DSS 처리군에서 유의적으로 감소하였다(p < 0.05). 이는 DSS 장염 모델에서 분변 내 SCFAs가 감소한다는 기존 보고들과 일치한다[36,37].
CMP의 단독 급여 효과는 acetate와 butyrate에서는 관찰되지 않았으나(p > 0.05), Day 6의 propionate 농도를 증가시키는 경향을 보였다(p = 0.06). 그러나 DSS 처리 조건 하에서 CMP는 상호작용을 통해 SCFAs 조성 변화에 유의적인 영향을 미쳤다. 특히 acetate의 경우, Day 3−4에서는 D군의 농도가 C군보다 낮았으나, Day 5−6에서는 반대로 증가하여 유의적인 상호작용이 확인되었다(p < 0.05). Propionate 또한 Day 4에는 D군에서 감소했으나 Day 5−6에는 C군보다 높은 수준을 보여 상호작용 효과를 나타냈다(p < 0.05). Butyrate 역시 Day 5−6에서 D군이 C군보다 유의적으로 높은 농도를 보여 CMP와 DSS 간의 상호작용이 확인되었다(p < 0.05).
분변 내 SCFAs 농도 감소는 염증성 장 질환 및 DSS로 유도된 대장염 모델에서 흔히 관찰되는 대사적 특징이다[38,39]. 본 연구에서 DSS 처리군(C, D군)의 SCFAs 농도 감소는 이러한 장 염증 특성과 일치한다. 장내 미생물이 생성하는 acetate, propionate, butyrate는 장 상피세포의 에너지 공급, 장벽 유지 및 면역 조절에 핵심적인 역할을 수행한다[37,40]. 특히 SCFAs 농도의 회복은 점막 치유, 항염증 반응 조절, 장내 미생물 균형 회복의 지표로 해석될 수 있다[39,41]. 기존 연구에서도 DSS 모델 마우스에게 600 mg/kg의 CM을 투여했을 때 acetate가 증가하거나[36], 돼지에게 300 mg/kg의 CM을 급여했을 때 결장 내 acetate와 butyrate가 향상된 바 있다[16]. 따라서 본 연구에서 관찰된 D군의 SCFAs 회복 효과는 CMP 급여가 DSS로 유도된 대장염을 완화하고, 장내 대사 환경 개선에 기여할 수 있음을 시사한다.
종합적으로 CMP 급여는 DSS로 인한 SCFAs 감소를 부분적으로 회복시킬 가능성이 있다. 다만 본 연구의 SCFAs 분석 결과만으로 CMP가 장 상피 구조 회복, 미생물 군집 변화, 염증 완화 기전에 직접적으로 기여했는지 단정하기는 어려우며, 향후 장 조직 병리, 장내 미생물 군집 분석 및 염증성 사이토카인 발현 등에 대한 추가적인 연구가 병행되어야 한다.
3.4. RT-qPCR
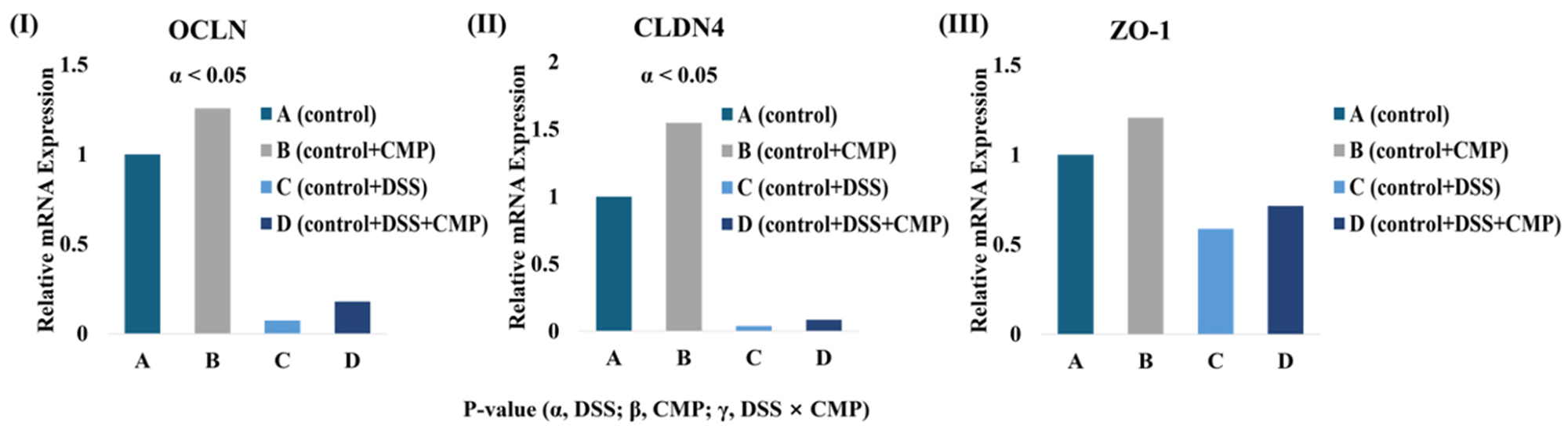
공장 조직 내 밀착연접 관련 유전자 발현 결과는 Fig. 3에 제시하였다. OCLN과 CLDN4의 발현은 DSS 처리에 의해 C, D군에서 유의적으로 감소하였다(p < 0.05). 반면, CMP 단독 급여 효과 및 CMP와 DSS 간의 상호작용 효과는 두 유전자 모두에서 관찰되지 않았다. 또한 ZO-1 유전자 발현은 DSS, CMP 처리 및 두 요인 간 상호작용에 의해 유의적인 영향을 받지 않았다. 이러한 결과는 DSS가 OCLN 및 CLDN4 발현을 감소시킨다는 기존 보고와 일치하며[42,43,44], 특히 ZO-1의 변화가 제한적이라는 연구 결과와도 부합한다[44].
Wu 등[18]은 2.5% DSS 모델에서 100 mg/kg CMP 경구 투여가 OCLN, CLDN1, ZO-1 발현을 증가시킨다고 보고하였으며, 돼지 대상 연구에서도 300 mg/kg CM 급여가 CLDN1과 ZO-1 발현을 향상시키는 것으로 나타났다[16]. 이 연구들에 따르면 CMP는 장 점막의 밀착연접 기능을 개선해 장 건강에 기여할 가능성이 있다. 그러나 본 연구에서는 CMP에 의한 유전자 발현 개선 효과가 관찰되지 않았다.
이러한 차이는 장염 유도를 위해 사용된 DSS 농도의 차이에서 기인했을 가능성이 있다. 본 연구에서 사용된 5% DSS는 중증 급성 장염을 유도하는 고농도로, 2−3% DSS를 사용한 선행 연구들에 비해 조직 손상 수준이 심각하고 회복 가능성이 제한적일 수 있다[45,46]. 따라서 극심한 점막 손상 상태에서는 CMP의 보호 효과가 유전자 발현 수준에서 충분히 나타나지 못했을 가능성이 있다. 또한 CMP의 투여 방식 차이 역시 영향을 미쳤을 수 있다. 선행 연구들이 CMP를 경구 투여한 반면, 본 연구에서는 음수에 혼합하여 자유 섭취하도록 하였다[18,32]. 이는 개체 간 CMP 섭취량의 변동을 초래할 수 있으며, 특히 기호성 저하로 인해 유효 농도에 도하지 못했을 가능성이 있다.