1. Introduction
2. Materials and Methods
2.1 실험동물 및 윤리 승인
2.2 PMSG 제조 및 투여
2.3 실험군 구성 및 처치 설계
2.4 체중 및 섭취량 측정
2.5 안락사 및 혈액 채취
2.6 백혈구 분석
2.7 NADH 및 Flavin 측정
2.8 SDS-PAGE 기반 혈청 Albumin 패턴 분석
2.9 조직 처리, 절편 제작 및 염색
2.10 통계 분석
3. Results
3.1 카페인 섭취 수준에 따른 마우스 자궁의 형태학적 변화 및 생활사 지표 분석
3.2 카페인 처리에 따른 혈액학적 변화 분석
3.3 카페인 처리에 따른 난소의 구성의 조직학적 특성 분석
3.4 카페인 처리에 따른 자궁과 질 점막의 조직학적 차이
4. Discussion
Conclusion
1. Introduction
암컷 포유류의 생식 기능은 시상하부 뇌하수체 난소 축을 중심으로 조절되며, 난소와 자궁의 정교한 신호 균형이 배란, 수정, 착상 가능성을 좌우한다[1]. 이 과정에서 난포는 성장과 퇴화, 배란 전 성숙의 단계를 거치며, 세포 생존과 사멸의 균형이 난포 운명을 결정하는 핵심 기전으로 작동한다[2]. 난포의 성장 신호는 PI3K AKT, MAPK, WNT, Notch, Hedgehog 등 다중 경로가 얽혀 있으며, 이들 신호가 과도하거나 비정상적으로 편향되면 난포 발달의 질적 저하와 생식 결과의 변동성이 커진다[3]. 특히 과배란 유도는 난소 반응을 인위적으로 증폭시키는 호르몬의 대표적 개입으로, 단기간에 다수 난포의 동시 성숙을 유도한다는 장점이 있으나, 난소와 자궁 미세환경을 생리적 범위 밖으로 밀어내는 위험을 동반한다[4].
과배란 조건에서는 난소 조직의 혈관 신생, 부종, 염증성 반응이 강화될 수 있으며, 이 과정에서 VEGF 신호 및 그 하위의 PKA 축은 병태 생리의 중요한 매개 축으로 제시되어 왔다[5]. 또한, 과배란은 난소와 초기 배아에서 지질 대사 프로파일을 변화시키고, 에너지 대사 재편과 연계된 스트레스 환경을 형성할 가능성이 보고되었다[5]. 반복적 과배란 자극은 생식관 조직에서 산화 환원 균형을 흔들고, peroxiredoxin 계열의 발현 변화 및 과산화 상태와 연계된 생체 반응이 관찰된 바 있다[6, 7]. 더 나아가 과배란 트리거 조건이 착상 단계의 자궁 반응성에까지 영향을 미칠 수 있으며, 자궁 리모델링, 이온 수송, 면역 관련 유전자 발현 변화가 착상 저해와 연결될 수 있다는 전사체 기반 근거도 제시되었다[8].
한편 에너지드링크 섭취는 청소년을 포함한 다양한 집단에서 증가 추세로 보고되며, 카페인이 주요 활성 성분으로 작용한다[8]. 카페인의 과다 섭취는 전신 대사와 산화 염증 경로에 영향을 주고, 조직 수준에서 스트레스 반응의 방향성을 바꿀 수 있다는 연구가 있으며[9, 10], 또한 카페인은 PI3K, AKT, mTOR의 생리 활성 메커니즘과 연결된 자가포식과 세포사멸 경로를 조절하여 세포 생존 전략을 재편할 수 있으며, 이는 생식 조직에서도 스트레스 환경에서의 세포 운명 결정에 영향을 줄 가능성이 있다[11].
동물 연구에서 임신기 카페인 노출은 난관 내 배아 이동과 자궁 수용성 저해와 연관되어[12] 임신 초기 난관 내 배아 수송과 배아 발달, 자궁 수용성에 악영향을 줄 수 있다는 연구가 보고되고 있다[10]. 이러한 데이터는 카페인이 단순한 각성 물질을 넘어 생식 과정의 미세한 단계에 개입할 수 있음을 시사한다[10].
하지만 현재까지의 연구는 과배란 또는 카페인 노출을 각각 다루는 경우가 많고, 과배란으로 유도된 난소 자극 환경에서 에너지드링크의 카페인 농도 차이가 난소 및 자궁에 미치는 영향을 체계적으로 비교한 근거는 충분하지 않다[13]. 카페인 고함량 음료에 대한 연구 중 보조원료인 타우린 및 당의 함량에 대한 부가적 작용은 카페인 작용에 큰 영향을 준지 않으며, 생리학적 변화에 미치는 영향 또한 미비한 것으로 알려져 있다[14].
즉 본 연구의 중점 요인인 카페인 음료의 생리학적 작용 분석에서 PMSG priming 기반의 난소 자극은 난포 발달과 성숙을 단기간에 활성 시키는 대표적인 과배란 시스템으로써, 카페인 음료에 고함량으로 첨가되어 있는 카페인과 같은 대사 활성 물질에 노출될 때 혈관 신생 반응, 산화 환원 균형, 난포 세포 사멸 및 자궁 수용성 관련 반응이 어떻게 작용하는지 확인할 필요가 있음을 시사한다[15, 16]. 따라서 본 연구는 ICR 암컷 마우스에서 PMSG priming 조건을 설정한 뒤, 각기 카페인의 함량이 다른 에너지드링크를 음수 하였을 때 난소와 자궁을 중심으로 생식 기관의 조직학적 변화와 생식 미세환경의 교란 가능성을 비교 평가하고자 한다.
2. Materials and Methods
2.1 실험동물 및 윤리 승인
본 연구는 한경국립대학교 동물생명윤리위원회의 승인을 받아 수행하였다(IACUC 승인번호 2025-3). 실험에는 7주령 암컷 ICR 마우스 9마리를 사용하였다(Nara Biotec, Pyeongtaek, Gyeonggi-do, Republic of Korea). 모든 개체는 실험 시작 전 1주간 적응 기간을 거친 후 처치를 시작하였다. 사육 환경은 항온·항습 조건에서 유지하였고, 실내 온도는 25°C 내외, 상대습도는 약 50%로 유지하였다. 동물은 개별 케이지에 수용하였고, 명암 주기는 12시간 명기와 12시간 암기로 유지하였다. 실험 기간 동안 일반 고형사료와 물을 자유급이로 제공하였다.
2.2 PMSG 제조 및 투여
PMSG(Sigma-Aldrich, St. Louis, MO, USA)는 5 IU/mL 농도로 증류수에 희석한 후 1CC 주사기를 이용해 개체당 0.1 mL를 하복강에 10일 동안 2틀에 한번씩 총 5회 주사하여 호르몬 변화를 유도하였다.
2.3 실험군 구성 및 처치 설계
본 연구에서 공시한 마우스는 카페인 첨가 에너지드링크에 따른 기관 수준 변화를 예비적으로 탐색하기 위한 파일럿 연구로 수행하였다. 이에 동물 사용 수를 최소화한다는 3R 원칙을 반영하고, 기관 변화의 경향성과 실험 가능성을 우선 확인하기 위하여 총 9마리의 마우스를 사용하였으며, 무작위 배정을 통해 3개 군에 각 3마리씩 배치하였다. 대조군은 PMSG 단독 처치를 수행하였고, 처리군은 PMSG 처치와 함께 카페인 함량이 다른 에너지드링크를 경구 투여하였다. 각 처리군에 따라 대조군(CON)은 PMSG만 처리 후 일반 음수를 경구 투여하였으며, 저카페인 음료 처리 군(GA)은 PMSG 처치 후 저카페인 에너지드링크를 경구 투여하였고, 고카페인 처리군(GB)은 PMSG 처치 후 고카페인 에너지드링크를 경구 투여하였다. 투여기간은 총 10일 동안 매일 1회 경구 투여하였다.
실험에 사용한 에너지드링크는 국내 유통 제품 중 카페인 함량 차이가 큰 에너지드링크를 설별하고, 이후 카페인 외 보조 물질의 함량이 생리학적 영향을 주지 않은 범위에 있는 에너지드링크를 McLellan 등[14]의 연구 결과를 토대로 2종의 에너지드링크를 선정하였다. 저카페인 제품은 250 mL당 카페인 60 mg, 고카페인 제품은 250 mL당 카페인 150 mg을 함유하였다. 에너지드링크의 투여량은 사람의 1회 섭취량인 250 mL를 기준으로, 선행연구[17]에 따라 체중 기준(mL/kg)으로 환산하여 설정하였다. 본 연구에서는 체표면적 보정 또는 열량 기준 환산은 적용하지 않았으며, 투여 기준은 4.5 mL/kg/day로 정하였다. 마우스의 평균 체중이 30 g이었으므로, 일일 투여량은 4.5 mL/kg × 0.03 kg = 0.135 mL/day로 계산하였다. 이에 따라 모든 실험동물에 대해 0.135 mL의 에너지드링크를 10일간 매일 1회 경구 투여하였다.
2.4 체중 및 섭취량 측정
사료 섭취량과 음수 섭취량은 실험 기간 동안 매일 측정하였다. 사료와 음수는 3일 주기로 오전 10시에 새로 제공하였고, 전일 제공량에서 잔량을 제외하여 군별 섭취량을 산출하였다. 산출된 값은 평균 일일 사료 섭취량과 평균 일일 음수 섭취량 계산에 활용하였다. 체중은 전자저울로 매일 동일 시간대에 측정하여 개체별 변화 양상을 기록하였다.
2.5 안락사 및 혈액 채취
실험 종료일 10일째에 모든 마우스를 24시간 절식시킨 뒤, 11일차 오전에 경추 탈골법으로 안락사하였다. 안락사 직후 복부를 에탄올로 소독한 후 심장 채혈로 혈액을 수집하였다.
2.6 백혈구 분석
혈액 5 µL를 취해 마이크로튜브로 옮긴 뒤, EDTA 5 µL를 첨가하여 응고를 방지하였다. 이후 CytoFlamma® CBC WBC/4D(Bioacts, Namdong-gu, Incheon, Kor) 10 µL를 전혈과 1:1로 섞어 반응시킨 후 백혈구 분석을 수행하였다. 혈액 분석은 자동 혈구분석기(WBC-5; Konsung, Jiangsu, China)를 사용하여 WBC, NEU, LYM, MON, EOS, BAS를 각각 분석하였다.
2.7 NADH 및 Flavin 측정
NADH 및 flavin 신호는 제조사 매뉴얼에 따라 마이크로플레이트 리더(Epoch; Agilent Technologies, Santa Clara, CA, USA)로 측정하였다. 본 측정은 NADH와 flavin 계열의 고유 형광 신호를 기반으로 대사 상태를 평가하는 기존 광학적 접근을 참고하여 수행하였다[18, 19].
2.8 SDS-PAGE 기반 혈청 Albumin 패턴 분석
혈청 내 albumin 패턴 확인을 위해 SDS-PAGE를 수행하였다. 개체별 혈청 5 µL를 취해 마이크로튜브로 옮긴 뒤, 5× protein loading buffer(Sigma-Aldrich, St. Louis, MO, USA) 5 µL를 첨가하여 혼합하였다. 12% SDS-PAGE 겔에 혼합액 10 µL를 분주하였고, 150 V에서 2시간 전기영동을 수행하였다. 분자량 마커는 Electrophoresis Marker(Sigma-Aldrich, St. Louis, MO, USA)를 사용하였다. 전기영동 후 겔을 분리하여 밴드 패턴을 확인하였다.
2.9 조직 처리, 절편 제작 및 염색
각 개체의 난소와 자궁 조직은 70% 에탄올로 탈수한 뒤 파라핀 포매(Sigma-Aldrich, St. Louis, MO, USA)를 수행하였다. 파라핀 블록은 마이크로톰(Microtome; RMC Boeckeler, Tucson, AZ, USA)으로 절편을 제작하였고, 절편 두께는 10 µm로 설정하였다. 파라핀 제거는 자일렌(xylene; Sigma-Aldrich, St. Louis, MO, USA)에 10분간 2회 침지하여 수행하였다. 이후 100% 에탄올과 95% 에탄올에서 각각 5분간 2회, 70% 에탄올에서 5분간 1회 반응시킨 뒤 증류수로 5분간 2회 세척하였다.
Alcian blue 염색은 3% 초산에서 3분간 전처리한 후, Alcian blue 용액(Alcian blue; Sigma-Aldrich, St. Louis, MO, USA)으로 30분간 반응시켰다. 염색 후 증류수로 5분간 세척하였고, Nuclear Fast Red(Sigma-Aldrich, St. Louis, MO, USA)로 5분간 대조염색한 뒤 증류수에서 1분간 추가 세척하였다.
H&E 염색은 hematoxylin-eosin 용액(Sigma-Aldrich, St. Louis, MO, USA)에서 30초 반응시킨 뒤, 70% 에탄올에서 5분간 세척하여 과잉 염색을 제거하였다. 모든 슬라이드는 95% 에탄올, 100% 에탄올, 자일렌 순으로 각 단계 5분씩 2회 반복 처리하여 탈수 및 투명화를 수행하였다.
이후 Mounting은 자일렌 20 µL와 permount(Sigma-Aldrich, St. Louis, MO, USA) 20 µL를 혼합하여 조직 위에 도포한 후 커버글라스를 덮어 건조하였다. 조직 관찰은 광학현미경(Ni2-U; Nikon, Tokyo, Japan)으로 각 40×, 200× 그리고 ROI(Region of Interest)로 조직학적 분석을 수행하였다.
2.10 통계 분석
통계 분석은 Microsoft Excel의 Data Analysis Toolpak(Microsoft, Redmond, WA, USA)을 이용하였다. 체중, 사료섭취량, 음수량 등 연속형 변수의 군 간 차이는 one-way ANOVA로 평가하였다. 초기값과 종료값의 변화는 paired t-test로 검정하였다. 분석 결과는 mean ± SD로 표시하였고, p ≤ 0.05를 유의수준으로 설정하였다.
3. Results
3.1 카페인 섭취 수준에 따른 마우스 자궁의 형태학적 변화 및 생활사 지표 분석
대조군(Con), 저카페인군(GA), 고카페인군(GB) 간 자궁의 해부학적 차이를 분석한 결과 육안적 형태가 서로 다르게 관찰된다. 대조군은 자궁체(uterus body)와 양측 자궁각(uterine horns)의 윤곽이 비교적 균형적으로 형성 되었으며, 부속 구조(난소, 난관)와 cervico–vaginal 구간의 해부학적 위치가 명확히 관찰되는 반면 GA 및 GB에서는 자궁각의 윤곽과 길이, 자궁체와 cervico–vaginal 구간의 외형이 대조군과 다른 양상으로 보이며, 특히 GB에서는 자궁각이 더 길고 가늘게 보이는 정성적 차이가 확인된다(Fig. 1A).
생활사 지표(time-course)에서도 군 간 차이가 특정 시점에서 확인된다. 체중은 Day 5에서 GA가 유의적으로 높은 평균값을 보였으며, 사료 섭취량은 Day 7에서 GA의 평균값 증가가 두드러졌다(Fig. 1B). 물 섭취량은 Day 8에서 대조군(Con)의 평균값이 유의적으로 높았다(Fig. 1B).
자궁 형태를 표준화하여 비교한 landmark 기반 도식으로 군별 형태 차이를 재현한 결과 자궁각과 cervico–vaginal 구간에 설정한 기준점(L1–L6)을 기반으로 윤곽을 중첩한 결과, Con, GA, GB가 서로 다른 윤곽 분포를 보이며, 이는 Fig. 1A에서 확인되는 육안적 형태 차이와 일관된 방향의 군별 기하학적 차이가 있음을 시사한다(Fig. 1C).
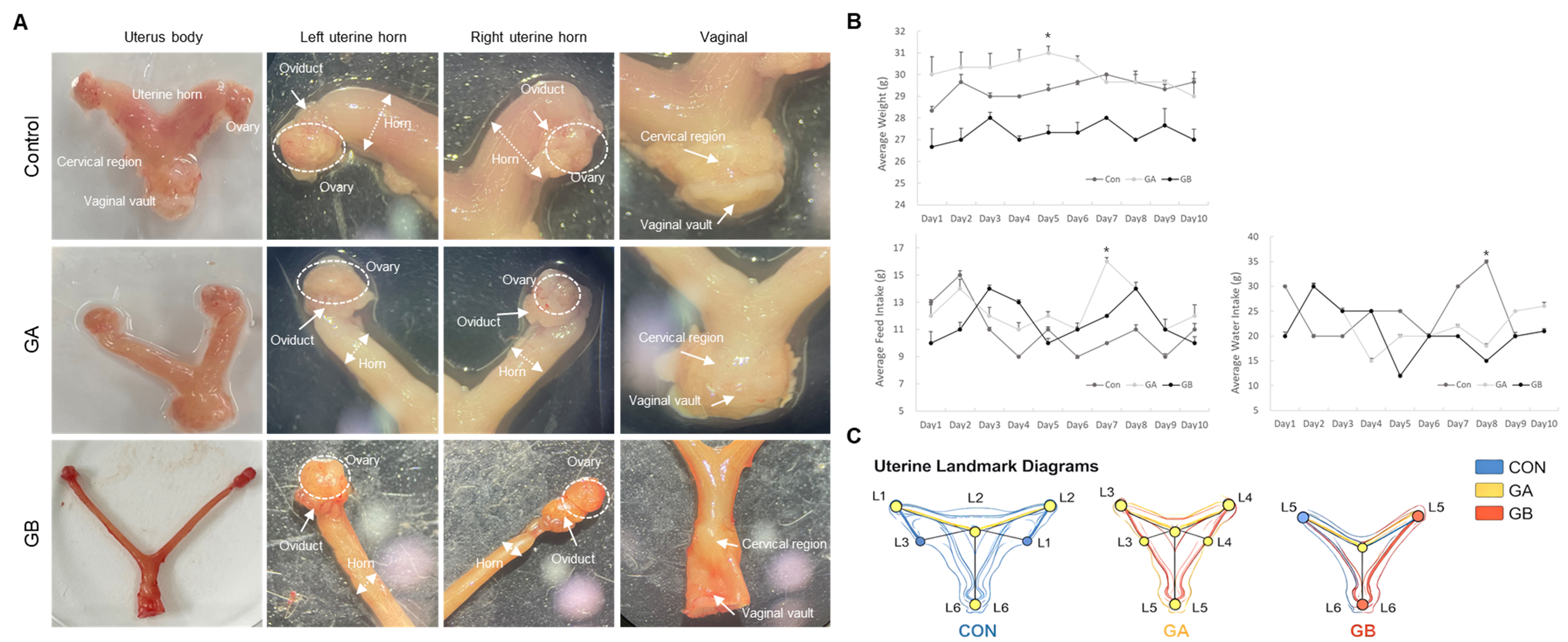
Fig. 1
Caffeine intake–associated differences in gross uterine morphology, life-history measures, and landmark-based uterine schematics. Con, control group; GA, low caffeine group A; GB, high caffeine group B. (A) Representative gross images of the excised female reproductive tract showing the uterus (uterine body and bilateral uterine horns) and the cervical-vaginal region; adnexal structures (ovary and oviduct) are indicated. (B) Time-course profiles of life-history measures during the experimental period, including average body weight, average feed intake, and average water intake. (C) Landmark-based uterine schematic diagrams for standardized comparison of uterine geometry across groups; anatomical landmarks (L1–L6) were placed at predefined reference points along the uterine horns and the cervical-vaginal region. *indicates a statistically significant between-group difference at the indicated time point (p ≤ 0.05), with the marked group representing the higher mean value at that time point.
3.2 카페인 처리에 따른 혈액학적 변화 분석
말초혈액 검사에서 총 백혈구 수(WBC)는 군 간 유의한 차이가 있었고, GB가 17.50 ± 0.68 (10³/µL)로 가장 높은 수준을 보였다(Table 1). 대조군(Con, 9.10 ± 1.04)과 GA(GA, 9.40 ± 1.96)은 평균값이 유사한 범위에 위치했다(Table 1).
백혈구 분획에서도 군 간 유의한 차이가 확인되었으며, GB에서 변화가 집중되는 양상이 나타났다(Table 1). 단핵구(MON)는 GB가 0.95 ± 0.17로 Con(0.46 ± 0.08) 및 GA(0.47 ± 0.72)보다 높은 수준을 보였으며, 호중구(NEU) 역시 GB가 13.78 ± 6.09로 Con(6.50 ± 1.39) 및 GA(6.64 ± 6.76)보다 유의적으로 높은 수준을 보였다(Table 1). 호산구(EOS)는 군 간 유의한 차이가 있었고, 평균값 기준으로 GB(0.35 ± 0.37)가 가장 높고 GA(0.19 ± 0.36)가 가장 낮은 수준을 보였다. 호염기구(BAS)도 군 간 유의한 차이가 있었으며, GB(0.05 ± 0.04)가 Con(0.01 ± 0.03)과 GA(0.02 ± 0.03)보다 높은 수준을 보였다. 림프구(LYM)는 GB(2.41 ± 6.29)에서 유의적으로 증가하였다(Table 1).
Table 1.
Peripheral white blood cell count and leukocyte differential in caffeine-treated mice
Con, control group; GA, low caffeine group A; GB, high caffeine group B. Total white blood cell count (WBC, ×10^3/μL) and leukocyte subtype values (LYM, lymphocytes; MON, monocytes; NEU, neutrophils; EOS, eosinophils; BAS, basophils) are presented as mean ± SD for Con, GA, and GB. Asterisks within each column indicate statistically significant differences among groups (*p ≤ 0.05, **p ≤ 0.01, as defined in the Statistical analysis).
혈액 기반 이미지 분석에서도 각 군별 차이가 있었다. 말초혈액 도말 표본에서 각 군의 백혈구 상대적으로 차이가 있었으며, GA와 GB에서 이상질적 세포체가 확인 되었다(Fig. 2B). 혈장 단백질 분석에서는 SDS-PAGE에서 군별 밴드 패턴이 서로 다른 양상으로 관찰되며, 특히 GB군에서의 globulin 영역과 주요 혈장 단백질 영역이 상대적으로 높았다(Fig. 2A).
내인성 신호 정량에서는 NADH와 flavin이 군별 유의적 차이를 보였다. NADH는 GA가 Con보다 유의적으로 높았고, GB는 GA보다 유의적으로 낮았다(Fig. 2C). 반대로 flavin은 GA가 Con보다 유의적으로 낮았고, GB는 GA보다 유의적으로 높았다(Fig. 2C). 즉, 카페인 처리 수준에 따라 환원성 신호(NADH)와 산화성 신호(flavin)의 상대적 균형이 군별로 다르게 이동하는 양상이 확인된다(Fig. 2C).
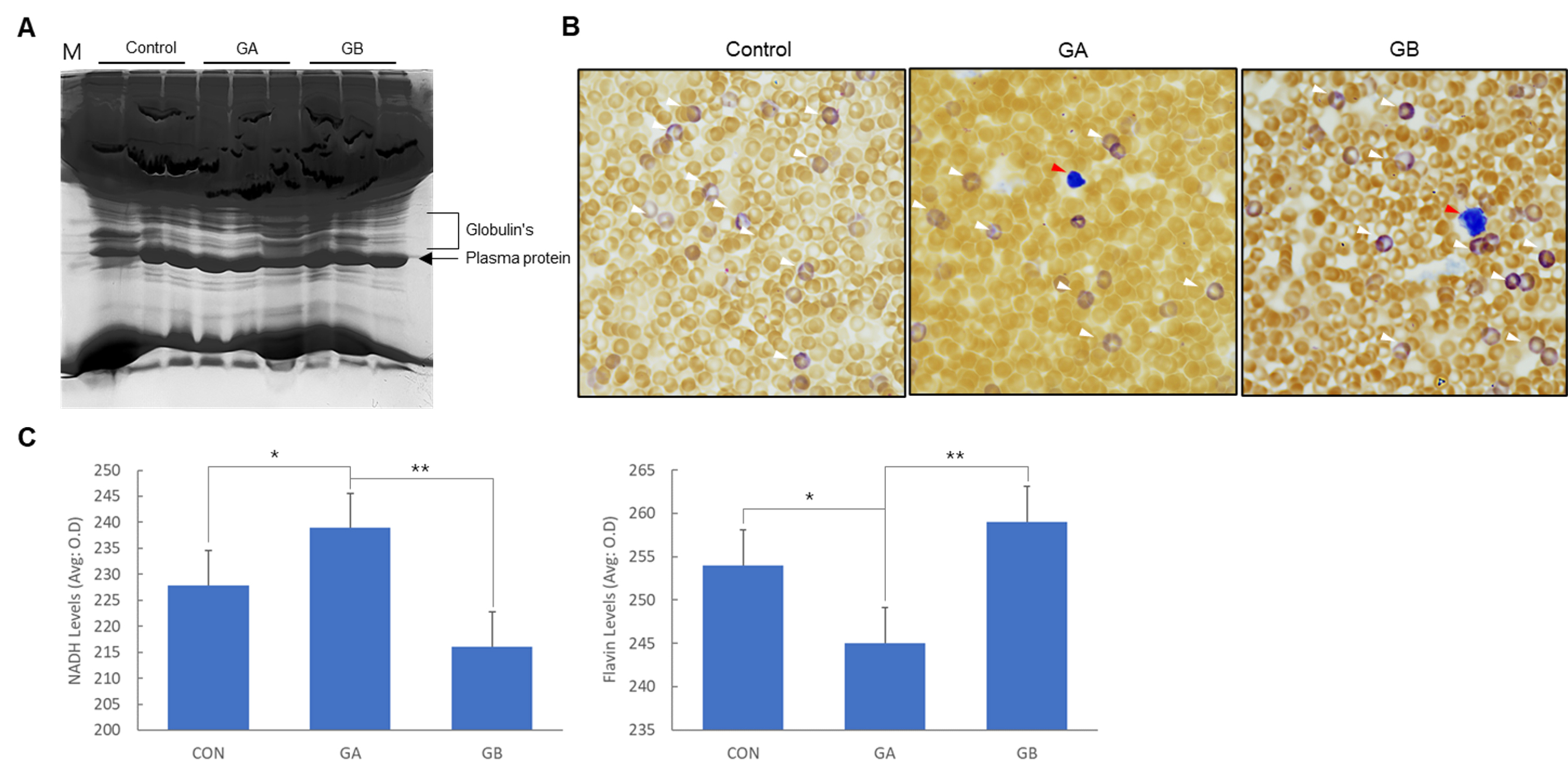
Fig. 2
Changes in plasma protein patterns, peripheral blood smear findings, and NADH and flavin signals in caffeine-treated mice. (A) Representative gel images of plasma proteins separated by SDS-PAGE, with major plasma protein bands and globulin regions indicated. (B) Representative microscopic images of peripheral blood smear specimens. White arrowheads indicate leukocytes, and colored arrows indicate representatively observed cells. (C) Results of quantification of NADH and flavin levels as mean optical density (O.D.). Bars represent the mean ± standard deviation. Con, control group; GA, low-caffeine group; GB, high-caffeine group. *p ≤ 0.05, **p ≤ 0.01.
3.3 카페인 처리에 따른 난소의 구성의 조직학적 특성 분석
난소에서는 카페인 처리군에서 난포 발달 상태와 황체(corpus luteum, CL) 구성의 양상이 대조군과 다르게 관찰된다. 도식화 분석에서 Con, GA, GB은 황체(CL), 난포(antral follicle, AF), 퇴화 난포(atretic follicle, At)의 분포 조합이 서로 다른 형태로 형성 되었다(Fig. 3A). H&E 염색에서 대조군은 난소 조직 내 황체와 함께 primary follicular 구조가 확인되며, 난포 구조가 명확히 관찰된다(Fig. 3B). 반면 GA과 GB에서는 발달 중 난포(develop follicular)와 황체가 함께 관찰되며, 난포 구조의 형태학적 변화가 군별로 다르게 나타났다(Fig. 3B). 즉, 카페인 처리 조건에 따라 난소의 난포 발달 단계와 황체 형성의 동반 양상이 군별로 차이가 있음을 확인 하였다(Fig. 3A, B).
각 처리 군에 따라 난관의 형성을 점막 주름과 상피 구조, 그리고 점액성 성분의 분포를 비교한 결과 GB군에서 난관의 형태학적 변화가 있음을 확인 하였다. Alcian blue 염색에서 각 군 모두 점막 주름(fold of mucosa)과 단층 원주상피(simple columnar epithelium) 및 고유판(lamina propria)이 서로 다르게 형성되어 있음을 확인하였으며, 특히 대조군에 비하여 카페인 섭취 군에서 점성 물질의 분포구간이 증가 되었다. 특히 GB군의 점막 영역에서 Alcian blue 양성 성분 상대적으로 높게 관찰된다(Fig. 3B). 군별로 점막 주름의 형태와 Alcian blue 양성 분포가 서로 다른 양상으로 나타나, 난관 점막 미세환경이 카페인 처리 조건에 따라 달라질 수 있음을 시사한다.
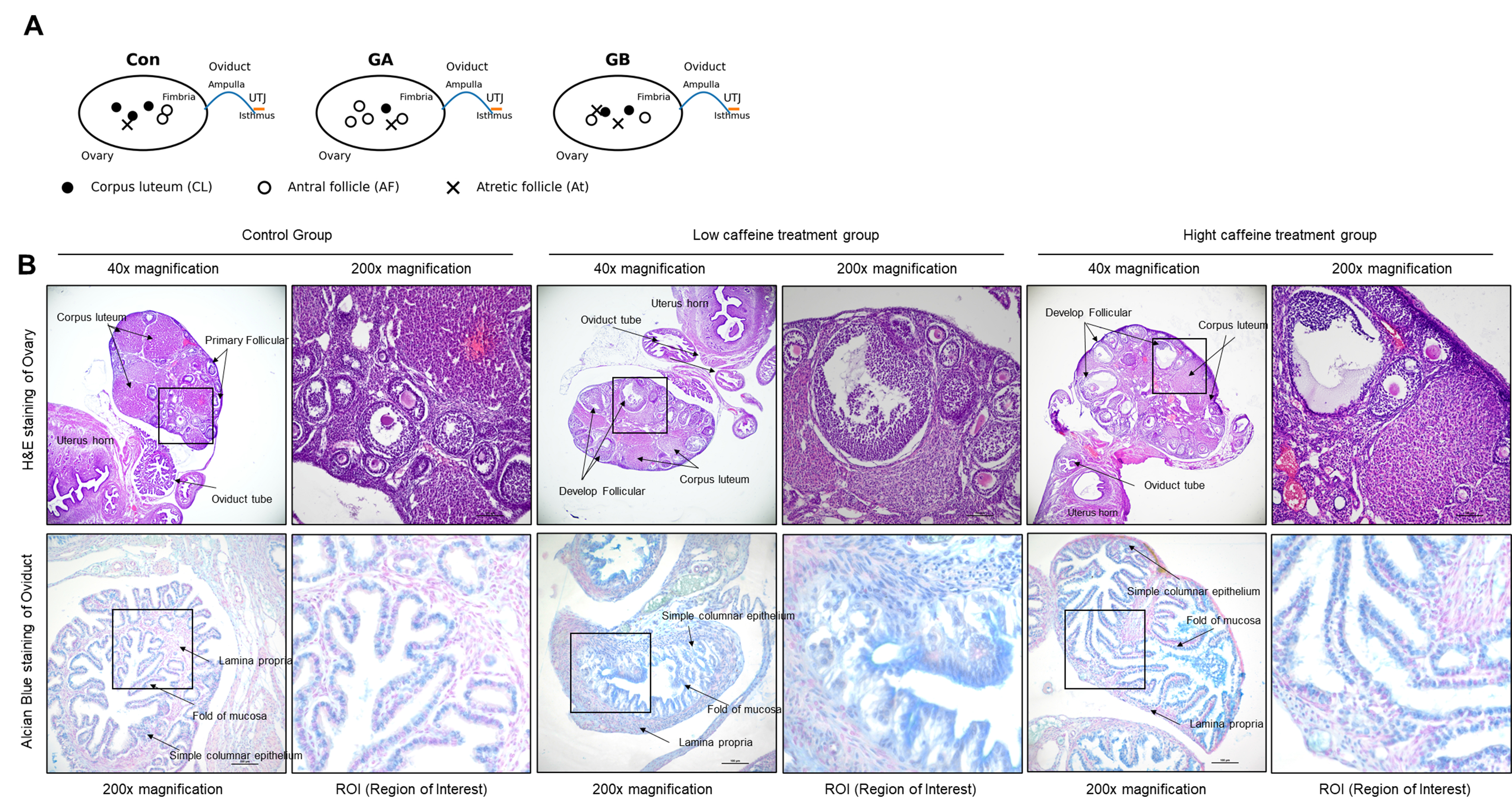
Fig. 3
Caffeine-associated differences in ovarian follicular structures and oviductal mucosa. (A) Schematic overview of ovarian structures in the control (Con), low-caffeine (GA), and high-caffeine (GB) groups. Symbols indicate corpus luteum (CL), antral follicle (AF), and atretic follicle (At); the oviductal segments (fimbria, ampulla, isthmus) and the uterotubal junction (UTJ) are illustrated. (B) Representative histological images of the ovary (H&E staining; 40× and 200×) and oviduct (Alcian Blue staining; 40× and 200×). Boxed regions indicate the regions of interest (ROI) shown at higher magnification.
3.4 카페인 처리에 따른 자궁과 질 점막의 조직학적 차이
자궁에서 형태학적 차이를 분석한 결과에서 모든 군에서 자궁내막(endometrium), 자궁선(uterine glands), 근층(myometrium), 자궁 내막선(stratum compactum)이 확인되었으며, 실험 군 모두 형태학적 차이가 있음을 확인 하였다(Fig. 4). 자궁선 구조와 내막 구성의 미세 형태가 Con에서는 균일한 형태를 가지는 반면 카페인 처리 군은 대조군에 비하여 낮은 발달을 보였으며, 내막 조직의 배열과 선 구조의 밀집 양상에 차이가 있다(Fig. 4). 특히 GB군은 자궁선과, 자궁내막선이 위축되어 있었으며, 자궁근층의 발달이 다른 군에 비하여 침밀하지 못한 형태를 띄었다. 이와 상반된 결과로 GA군의 경우 대조군과 비슷한 형태를 보이며, 자궁외막 근층의 발달이 GB에 비하여 두드러지게 발달 되어 있었다. Alcian blue 염색에서는 내막 영역에서 점액성 성분이 관찰되며, 군별로 염색 분포와 조직 배경의 양상이 다르게 나타났는데, 카페인 처리 조건에 따라 자궁 내막-선 구조 및 점액성 성분의 대조군에 비하여 증가 하였으며, 자궁내막선에 주로 분포 되었다(Fig. 4).
각 실험군의 질에서는 형태학적 분석 결과 각 군 모두 질 상피(vaginal epithelium)와 점액층(mucoid layer)이 확인되었으며, 큰 차이를 보이지 않았다(Fig. 4). 그러나 Alcian blue 분석에서 점액층 및 주변 조직에서 대조군에 비하여 GA, GB군에서의 점액성분 분포가 증가 하였으며, GA군에서 Alcian blue 양성 성분 매우 높게 분포 되었다(Fig. 4). 군별로 점액층의 형태와 Alcian blue 양성 분포가 서로 다른 양상으로 나타나, 질 점막의 점액성 미세환경 또한 처리 조건에 따라 달라짐을 확인하였다(Fig. 4).
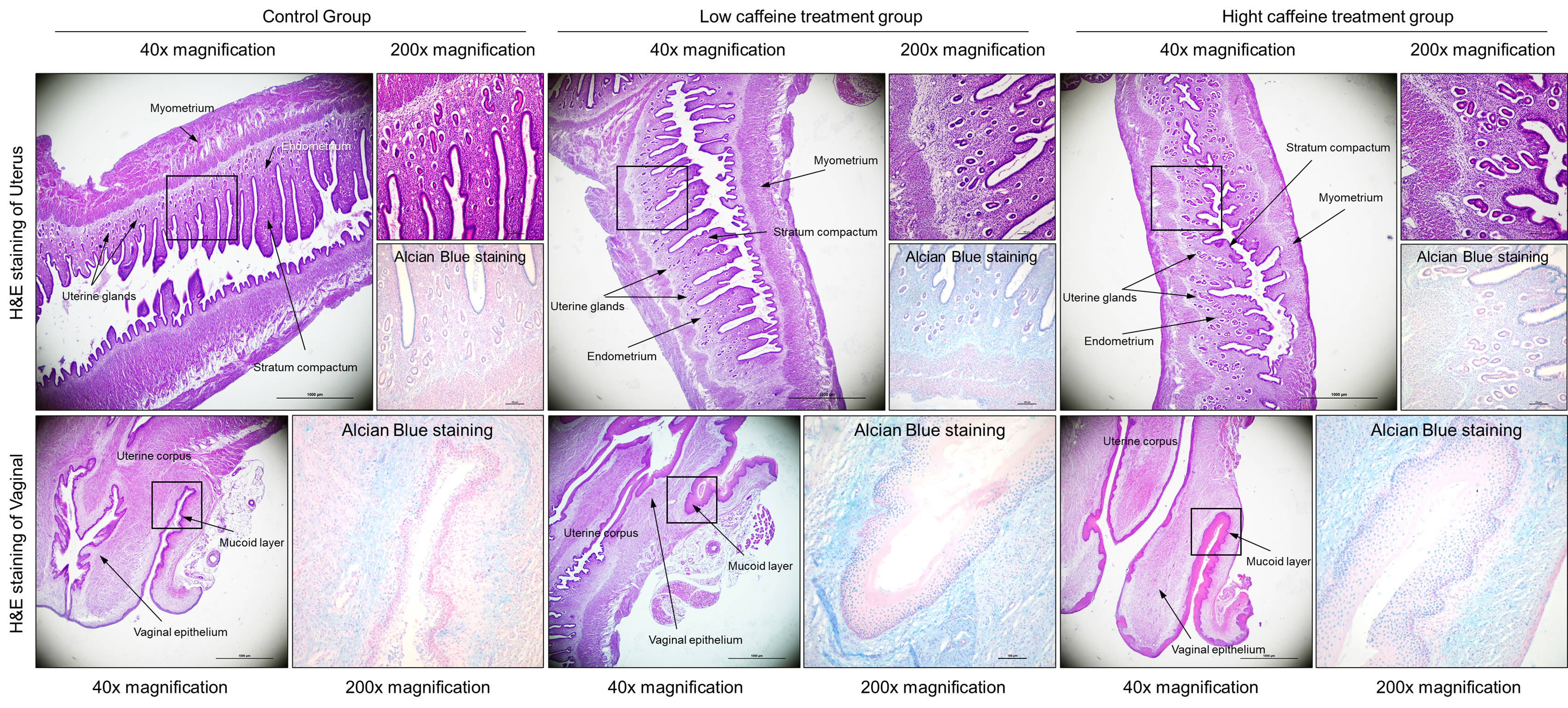
Fig. 4
Caffeine-associated histological differences in the uterus and vagina. Representative histological images of the uterus and vagina from the control (Con), low-caffeine (GA), and high-caffeine (GB) groups. Uterine sections are shown with H&E staining at 40× and 200× (top row), with boxed regions indicating the regions of interest (ROI). Vaginal sections are shown with H&E staining at 40× and Alcian Blue staining at 200× (bottom row). Key anatomical features (e.g., endometrium, myometrium, uterine glands/stratum compactum, vaginal epithelium, and mucoid layer) are indicated where applicable.
4. Discussion
본 연구는 PMSG 호르몬을 통해 생식반응을 교란 시킨 후 카페인 함량이 서로 다른 에너지드링크 섭취 조건에서 마우스의 전신 대사 변화와 생식기관의 형태학적 변화를 함께 평가하여, 생식 기능 저하로 이어질 수 있는 조직 수준의 단서를 제시하고자 하였다. 에너지드링크의 주요 기능성 성분으로 알려진 카페인은 교감신경계 자극과 대사율 변화를 통해 에너지 항상성에 영향을 줄 수 있으며, 이러한 대사 변화는 호르몬의 교란으로 인한 생식기능의 저하 혹은 생식 메커니즘의 변화와 연결될 수 있다[20, 21]. 즉 본 연구의 핵심은 대조군에 비하여 고카페인군 섭취군에서 자궁 및 백혈구의 변화가 가장 뚜렷했고, 저카페인군 섭취군은 같은 방향의 변화가 나타나더라도 강도는 상대적으로 낮았다는 점이다.
이러한 결과는 에너지드링크 노출의 생리학적 영향이 단순한 각성 효과를 넘어 호르몬 자극 상태의 대사 및 생식기관 항상성에 영향을 미칠 수 있음을 시사하며[9, 22], 특히 그 변화의 크기가 카페인 함량이 높은 조건에서 더 크게 나타났다는 점에서 카페인 농도 차이가 주요 설명 인자일 가능성을 뒷받침한다.
대사 지표에서 관찰된 체중, 사료 섭취량, 수분 섭취량의 군 간 차이는 카페인의 전형적인 생리 작용과 정합성이 있다[23]. 카페인은 식욕과 에너지 균형에 관여하는 신경내분비 경로를 통해 섭취 행동을 변화시키고, 에너지 대사를 재배치할 수 있다[3,11]. 본 연구에서 카페인 섭취군에서 사료 섭취량 저하 및 자궁의 변화가 뚜렷하게 관찰된 결과는 난소 스테로이드 환경, 난포 성장의 지속성, 그리고 착상 전후 자궁 미세환경의 안정성에 영향을 줄 수 있음을 시사한다[24, 25]. 특히, 고카페인 조건에서 나타난 대사 재편은 난소와 자궁이 요구하는 정교한 호르몬-대사 동기화를 깨는 방향으로 작동했을 가능성이 높다[4]. 특히 에너지음료의 보조 첨가제에 관한 기존 연구에서는, 타우린이나 당류 등 카페인 외 성분이 독립적으로 일관된 생리적 효과를 나타낸다는 근거가 제한적이며[14, 25], 전체 효과의 중심은 주로 카페인에 의해 설명된다고 보고된 바 있으며, caffeine, taurine, glucose를 분리해 평가한 연구에서도 인지 및 반응성과 관련된 주요 효과는 주로 카페인에 의해 작용 한다[14, 24]는 보고와 같이 카페인 첨가 함량에 따른 차이가 있음을 시사한다.
또한 전혈 분석에서 고카페인군에서 백혈구와 호중구 증가가 두드러진 점은, 고카페인 섭취가 전신 수준의 스트레스성 면역 반응 또는 염증성 톤의 상승과 맞물렸음을 보여준다. 카페인은 아데노신 수용체 길항과 교감신경 활성화와 연동되어 다양한 염증·산화 스트레스 축에 영향을 줄 수 있으며[3, 26], 여성 생식계에서는 호르몬 변화와 함께 난소 및 자궁 기능 지표의 교란으로 이어질 수 있다는 보고가 있다[21]. 과배란 유도 자체가 생식기관에 산화적 부담과 조직 리모델링 압력을 가하는 조건이라는 점을 고려하면[5,27], 에너지드링크 노출이 이러한 반응을 증폭했을 가능성이 있다. 즉 고카페인군에서의 면역세포 변화는 고카페인 에너지드링크 제품 노출이 호르몬 자극 상태의 마우스에서 면역계 변화를 동반할 수 있음을 보여주는 탐색적 소견으로 면역세포 변화가 “독립 사건”이 아니라 호르몬 자극과 카페인 자극이 겹치면서 나타난 전신 반응의 결과로 보는 해석이 더 설득력 있다.
혈장 내 NADH 및 flavin 신호 변화는, 대사 및 산화환원 상태의 군 간 차이를 간접적으로 뒷받침한다. 고카페인군에서 NADH 신호가 낮고, flavin 신호가 높은 결과를 보이는 반면 대조군과 저카페인군에서는 낮은 신호를 보이는 양상은, 전신 대사 환경이 상대적으로 산화된 방향으로 기울었을 가능성을 시사한다. 이 변화는 과배란 유도 조건에서 보고되는 산화 스트레스 증가 및 항산화 시스템 부담과 연결해 해석할 수 있다[4, 28]. 동시에 혈장 단백질 프로파일에서 뚜렷한 변화가 관찰되지 않았다는 점은, 본 모델에서의 변화가 “혈장 단백질의 대규모 손상/분해”보다는 대사·염증·조직 리모델링 축의 기능적 재조정에 더 가까웠음을 시사한다. 다만 그 유도 인자는 카페인 자체일 수도 있고, 당류 및 기타 첨가성분을 포함한 제품 전체 조성의 차이일 수도 있으나 기존의 연궁에 따라 보조 첨가물의 작용은 조직의 생리학적 변화를 유도하기에는 매우 낮은 수준일 수 있을 것이라 사료된다[14].
난소 조직에서 고카페인군의 난포 발달 균형이 흔들리고, 정상적인 배란과 황체 형성에 교란으로 황체와 거대난포가 동시에 발달되는 양상이 관찰되었다. 이는 과배란 유도 모델에서 흔히 논의되는 난소 과자극 상태의 병태생리와도 맞닿아 있다[5]. 난포기의 발달은 과립막세포의 생존 및 사멸 프로그램에 의해 결정되며, 과립막세포 apoptosis는 난포 위축과 배란 효율 저하를 설명하는 핵심 기전이다[28]. 카페인이 apoptosis 및 autophagy 신호를 조절할 수 있다는 보고[28, 29]를 고려하면, 고카페인 조건에서 난포 미세환경이 성장 유지보다는 소모 및 위축에 유리하게 재편되었을 가능성이 있다. 또한 반복적 과배란 유도에서 생식기관 전반의 항산화 단백질(예: peroxiredoxin)의 과산화/과부하가 보고된 바 있고[8], 본 연구의 고카페인군에서 관찰된 난소 변화는 이러한 산화적 부담이 심화된 조건에서 더 쉽게 나타날 수 있는 결과로 해석할 수 있다.
자궁 및 난관 조직에서 관찰된 구조적 변화와 점액성/당단백 기반 염색 패턴의 변화는, 수정란 이동과 착상 전 자궁 수용성에 중요한 의미를 갖는다[29]. 자궁과 난관은 단순 통로가 아니라, 상피와 분비 환경이 수정란 발달 단계별 요구에 맞춰 조절되는 기능성 장기이다[30]. 특히 자궁선은 자궁강 액체 항상성 및 착상 수용성에 직접 관여하며, 자궁선 기능 이상은 착상 실패로 연결될 수 있음이 동물모델에서 명확히 제시되어 왔다[31]. 카페인 섭취가 초기 임신에서 난관 내 수정란 이동과 자궁 수용성을 교란할 수 있다는 보고[32]는, 본 연구에서 고카페인군에서 관찰된 자궁·난관 미세환경 변화가 단순 조직학적 차이를 넘어 생식 성공률에 영향을 줄 수 있는 기능적 변화임을 지지한다[36]. 또한 에스트로겐은 자궁의 수분 이동 및 상피 기능 단백질(예: aquaporin) 발현을 조절하는데[34, 35], 본 연구처럼 과배란 유도 상태에서 대사·염증 반응이 동시에 변화하는 경우, 자궁 상피-기질의 균형이 쉽게 무너져 수용성 중심의 미세환경이 유지되기 어렵다. 그러나 이러한 조직학적 변화가 저카페인군보다 고카페인군에서 더 뚜렷하게 나타났다는 점은, 적어도 본 실험 조건에서는 카페인 함량이 높은 제품이 생식기관 미세환경을 더 크게 교란할 가능성을 시사한다.
종합하면, 과배란 유도 마우스에서 에너지드링크 섭취는 전신 대사, 면역세포 분포, 산화환원 균형, 그리고 난소·자궁·난관의 조직학적 변화와 관련된 일관된 변화를 보였으며, 그 변화의 강도는 저카페인군보다 고카페인군에서 더 크게 나타났다[34]. 이러한 양상은 호르몬 자극 상태에서 카페인 함량이 높은 에너지드링크 제품이 생식기관이 요구하는 항상성 조건을 교란할 수 있음을 시사한다[33, 36]. 본 연구는 유전적 또는 분자적 기전을 직접 규명한 것은 아니며, 상용 제품 간 비교 설계라는 한계가 있으나, 최소한 고카페인 제품 노출이 백혈구 분포 변화와 생식기관 미세환경 변화와 더 밀접하게 연관될 가능성을 제시한다.
Conclusion
본 연구는 PMSG로 과배란을 유도한 7주령 ICR 암컷 마우스에서 에너지음료 기반 카페인 섭취가 전신 대사, 면역 반응, 그리고 난소·자궁 조직 형태에 미치는 영향을 평가하였다. 카페인 섭취는 섭취 행동과 체중 변화 양상을 바꾸었고, 고카페인 조건에서는 백혈구 증가와 함께 염증성 반응이 강화되는 소견이 나타났다. 또한 난소에서는 난포 발달 및 황체 형성 양상이 교란되었고, 자궁·난관에서도 조직학적 변화가 동반되어 생식 미세환경의 안정성이 저하될 가능성을 시사하였다. 따라서 과배란과 같은 호르몬 자극 환경에서 고카페인 에너지음료 섭취는 생식 기능에 불리한 요인이 될 수 있다.




